Что такое коррозия?
При контакте металлического материала с окружающей средой происходит разрушение материала вследствие химического или электрохимического воздействия.
Коррозия – опасная и чрезвычайно дорогостоящая проблема. Из-за нее могут обрушиться здания и мосты, повреждаться нефтепроводы, она может служить причиною утечек на химических заводах, и т.д.. Корродированные электрические контакты могут вызвать пожары и другие проблемы, корродированные медицинские имплантаты могут привести к заражению крови, а загрязнение воздуха нанесло коррозионный ущерб произведениям искусства по всему миру. Коррозия угрожает безопасному захоронению радиоактивных отходов, которые необходимо хранить в контейнерах в течение десятков тысяч лет.
 Рисунок 1. Коррозия является одним из наиболее разрушительных и дорогостоящих природных явлений, наблюдаемых сегодня.
Рисунок 1. Коррозия является одним из наиболее разрушительных и дорогостоящих природных явлений, наблюдаемых сегодня.
Наиболее распространенные виды коррозии возникают в результате электрохимических реакций. Общая коррозия возникает, когда большинство или все атомы на одной металлической поверхности окисляются, повреждая всю поверхность. Большинство металлов легко окисляются: они имеют тенденцию отдавать электроны кислороду (и другим веществам) в воздухе или воде. Когда кислород восстанавливается (приобретает электроны), он образует оксид с металлом.
Когда восстановление и окисление происходят на поверхностях разных металлах, находящихся в контакте друг с другом, то процесс называется гальванической коррозией. Электролитическая коррозии, чаще всего возникает в электронном оборудовании,когда вода или другая влага задерживается между двумя электрическими контактами, между которыми существует электрическое напряжение. В результате получается самопроизвольная электролитическая ячейка.
Природа большинства коррозионных процессов электрохимическая. Электрические свойства границы раздела металл/раствор электролита (двойной электрический слой) широко используются в исследованиях механизма коррозии, измерении коррозии и мониторинге промышленной коррозии. Электрохимические методы, обычно используемые в исследованиях коррозии металлов, включают: потенциал разомкнутой цепи (OCP), поляризационную кривую (график Тафеля), электрохимический импеданс (EIS).
Методы исследования коррозии
Потенциал разомкнутой цепи (OCP)
На изолированном металлическом электроде одновременно с одинаковой скоростью протекает одна анодная реакция и одна катодная реакция, что называется сопряжененными электродными реакцииями. Реакция взаимного соединения называется «реакцией сопряжения», а вся система — «сопряженной системой». В сопряженной системе две электродные реакции взаимодействуют друг с другом, и когда потенциалы электродов равны, они не изменяются со временем. Это состояние называется «стабильным состоянием», а соответствующий потенциал — «стабильным потенциалом». В коррозионной системе этот потенциал также называется «потенциалом (само)коррозии Ecorr» или «потенциалом разомкнутой цепи (OCP)», а соответствующая плотность тока называется «плотностью (само)коррозионного тока icorr». Вообще говоря, чем более положителен потенциал разомкнутой цепи, тем труднее терять электроны и подвергаться коррозии, что указывает на лучшую коррозионную стойкость материала.
Потенциостаты-гальваностаты Corrtest серии CS могут использоваться для мониторинга электродного потенциала металлического материала в системе в режиме реального времени в течение длительного времени. После стабилизации потенциала можно получить потенциал разомкнутой цепи материала.
Поляризационная кривая (график Тафеля)
Явление, при котором потенциал электрода отклоняется от равновесного потенциала при прохождении через него тока, называется “поляризацией”. В электрохимической системе, когда происходит поляризация, отрицательное отклонение электродного потенциала от равновесного называется “катодной поляризацией”, а положительное отклонение электродного потенциала от равновесного называется “анодной поляризацией”.
Чтобы найти поляризационные характеристики электродного процесса, необходимо экспериментально определить перенапряжение или потенциал электрода как функцию плотности тока, которая называется «кривой поляризации».
Прямое измерение Icorr невозможно. Небольшие внешние сдвиги потенциала (E) будут продуцировать умеренное течение тока (I) на разрушаемом электроде. Динамика навязанным извне током определяется, как Icorr, по степени влияния, с которыми происходят анодные и катодные процессы. Чем больше влияние, тем меньше значение Icorr , и тем меньше значение I для данного изменения потенциала. На самом деле, при малых значениях E, I прямо пропорционален Icorr и, следовательно, скорости коррозии. Эти отношения, воплощены в теоретическом уравнении Штерна-Гири:
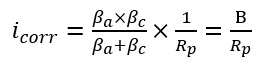
где: B - коэффициент Штерна-Гири материала, Rp - сопротивление поляризации металла.
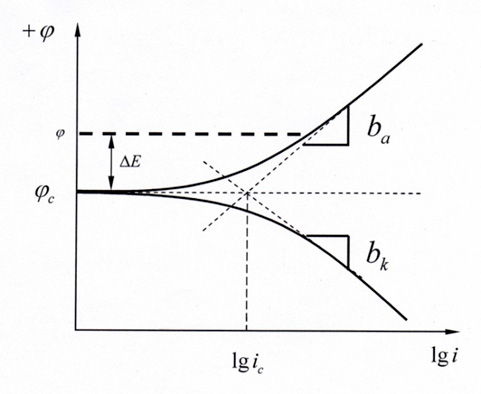
Принцип получения icorr с помощью метода экстраполяции по Тафелю.
Программное обеспечение Corrtest CS studio может автоматически выполнять подгонку поляризационной кривой. Что позволит определить коэффициенты Тафеля на анодном и катодном участках, т.е. ba и bc. а также затем получить icorr. Основываясь на законе Фарадея и в сочетании с электрохимическим эквивалентом материала, мы можем определить корость коррозии металла (мм/год).
Электрохимический импеданс
Техника электрохимического импеданса, также известная как импеданс на переменном токе, измеряет изменение напряжение (или ток) электрохимической системы в зависимости от времени, контролируя ток (или напряжение) электрохимической системы как функцию синусоидального изменения во времени. Измеряется полное сопротивление электрохимической системы, и далее изучается механизм реакции системы (среда/пленка покрытия/металл), а затем анализируются электрохимические параметры соответствующей исседуемой системы.
Спектр импеданса представляет собой кривую, построенную на основе данных импеданса, измеренных с помощью потенциостата с модулем измерения импеданса на разных частотах, а спектр импеданса электродного процесса называется спектром электрохимического импеданса. Существует много типов отображения спектра EIS, но наиболее часто используются график Найквиста и график Боде.
Пример экспериментов
В качестве примера приводится статья, опубликованная пользователем, использующим одноканальный потенциостат–гальваностат–FRA CS350M, в которой дается конкретное представление о методах системы измерения коррозии металлов.
Пользователь изучал коррозионную стойкость стентов из сплава Ti-6Al-4V, изготовленного традиционным методом деформирования (образец № 1), методом селективного лазерного плавления (образец № 2) и методом электронно-лучевого плавления (образец № 3). Стент используется для имплантации человеку, поэтому коррозионная среда представляет собой имитацию жидкости внутренней среды организма (SBF). Температуру экспериментальной системы также необходимо поддерживать на уровне 37 ℃.
Оборудование: одноканальный потенциостат–гальваностат–FRA CS350M
Вспомогательное оборудование: ячейка для изучения плоских образцов, термостатируемая, сушильная печь.
Используемые материалы: Ацетон, SBF, эпоксидная смола, отверждающаяся при комнатной температуре.
Экспериментальная среда:
Имитированная жидкость организма (SBF): NaCl - 8.01, KCl - 0.4, CaCl2 - 0.14, NaHCO3 - 0.35, KH2PO4 - 0.06, глюкоза - 0.34, единица измерения: г/л.
Образец (WE):
Стент из сплава Ti-6Al-4V размером 20×20×2 мм,
Активная площадь рабочего электрода 10×10 мм.
Неактивная зона покрыта/герметизирована эпоксидной смолой, отверждающейся при комнатной температуре.
Электрод сравнения (RE): Электрод сравнения насыщенный каломельный Hg/Hg2Cl2.
Вспомогательный электрод (CE): Платиновый электрод, сетка
 Рисунок 2. Внешний вид ячейки для изучения плоских образцов, термостатируемая.
Рисунок 2. Внешний вид ячейки для изучения плоских образцов, термостатируемая.
Этапы эксперимента и настройка параметров
Для получения более полной информации об обсуждаемых ниже методах и их параметров, используйте Руководство пользователя одноканальными потенциостатами серии Corrtest CS (eng)
Потенциал разомкнутой цепи (OCP)
Перед тестированием рабочий электрод необходимо отполировать (используя порошки оксида алюминия различной дисперсии, последовательно от грубой до тонкой: 360 меш, 600 меш, 800 меш, 1000 меш, 2000 меш по порядку), пока поверхность не станет гладкой. После полировки промойте его дистиллированной водой, затем обезжирьте ацетоном, поместите в сушильный шкаф и высушите при 37 ℃ для дальнейшего использования.
Вставьте образец в коррозионную ячейку, введите модельную жидкость организма в сосуд коррозионной ячейки и вставьте насыщенный каломельный электрод (SCE) с солевым мостиком в свободный порт электрохимической ячейки. Убедитесь, что кончик капилляра Луггина обращен вправо к поверхности рабочего электрода. Температура раствора внутри ячейки поддерживается на уровне 37℃ за счет циркуляции воды.
Соедините электроды с потенциостатом с помощью кабеля ячейки.
Затем: Experiment → stable polarization → OCP
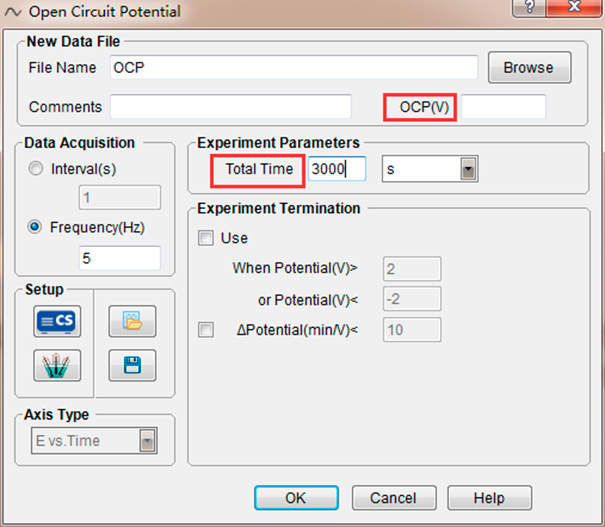
Задайте имя файла для сохранения данных, общее время тестирования и затем запустить тест. Потенциал OCP металлического материала в растворе меняется медленно, и для его стабилизации требуется относительно продолжительный период. Поэтому рекомендуется устанавливать время не менее 3000 секунд.
Поляризационная кривая
Experiment → stable polarization → potentiodynamic
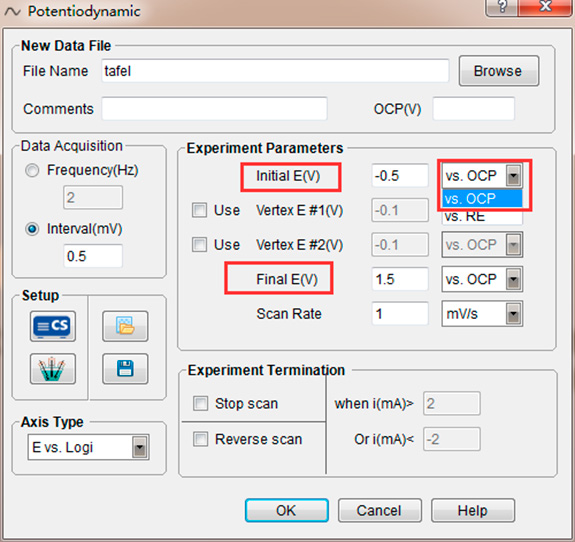
Задайте initial «E(V)» (начальный потенциал), «Final E(V)»(конечный потенциал) и «Scan Rate» (скорость сканирования), выберите точку отсчета для потенциала как «vs. OCP».Нажмите флаговую кнопку «Use» Iиспользовать), чтобы задать обортные потенциалы Vertex E#1 и Vertex E#2. Если оставить флаговую кнопку не активной, то потенциал при развертке не будет проходить соответствующие потенциал.
Следует отметить, что измерение поляризационной кривой может быть выполнено только при условии, что потенциал OCP уже стабилен. Для автоматического отслеживания стабильности потенциала OCP, используйте функцию OCP stable, нажав на следующую кнопку:
Программное обеспечение автоматически начнет измерение поляризационной кривой после того, как колебания потенциала OCP станут меньше 10 мВ/мин.
В этом примере эксперимента пользователь установил потенциал -0.5 ~ 1.5 В (vs. OCP).
Вы можете установить условие для остановки или обратного сканирования. В основном это используется для измерения потенциала точечной коррозии и измерения кривой пассивации.
Результаты
Потенциал разомкнутой цепи (OCP)
С помощью измерения потенциала разомкнутой цепи мы можем получить значение потенциала свободной коррозии Ecorr, по которому можно судить о коррозионной стойкости металлического материала. В целом, чем выше значение Ecorr, тем сильнее материал подвержен коррозии.
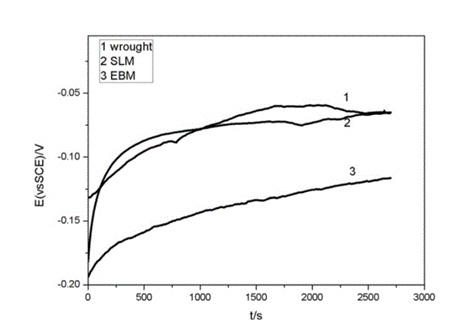 Рисунок 7. где: 1 - Стент из сплава Ti-6Al-4V, изготовленный традиционным методом деформирования; 2 - Стент из сплава Ti-6Al-4V, изготовленный методом селективного лазерного плавления; 3 - OCP стента из сплава Ti-6Al-4V, изготовленного методом электронно-лучевой плавки.
Рисунок 7. где: 1 - Стент из сплава Ti-6Al-4V, изготовленный традиционным методом деформирования; 2 - Стент из сплава Ti-6Al-4V, изготовленный методом селективного лазерного плавления; 3 - OCP стента из сплава Ti-6Al-4V, изготовленного методом электронно-лучевой плавки.
Из графика можно сделать вывод, что коррозионная стойкость образцов №1 и 2 лучше, чем у образцов №3.
Анализ графика Тафеля (измерение скорости коррозии)
Поляризационные кривые, полученные на исследуемых образцах, представлены ниже:
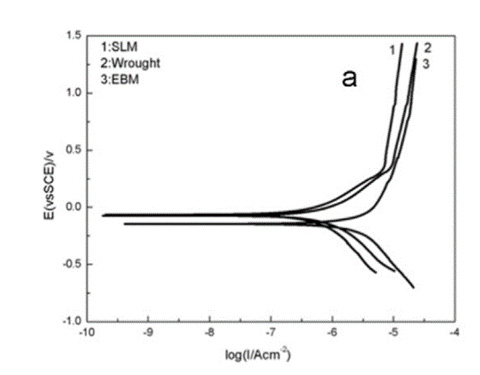
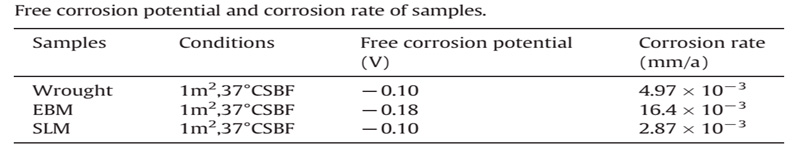
Как видно, из рассчитанного значения скорости коррозии мы можем сделать тот же вывод, что и при измерении методом OCP. Скорость коррозии рассчитывается по графику Тафеля.
Основываясь на графике Тафеля, мы можем получить плотность тока коррозии Icorr с помощью инструмента analysis fitting, встроенного в программное обеспечение CS Studio. Затем, в соответствии с другими параметрами, такими как площадь рабочего электрода, плотность материала, эквивалентный вес, рассчитывается скорость коррозии.
Шаги таковы:
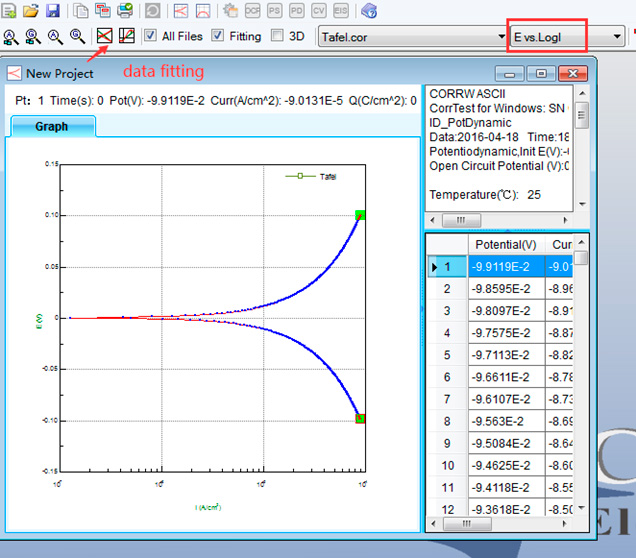
Подгонка данных:
Нажмите "Cell info" (Информационные данные об ячейке) и введите соответствующие значения.
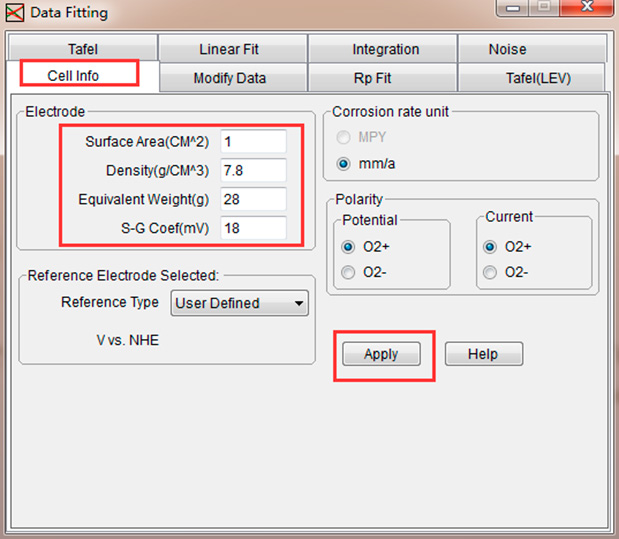
Если вы уже задали эти параметры в настройках ячейки и электродов перед тестированием, вам не нужно задавать здесь информацию о ячейке.
Нажмите на вкладку «Tafel» окна Data fiting. Выберите auto fit Tafel или подгонку для данных анодного/катодного отрезков вручную, после чего можно получить плотность тока коррозии, потенциал свободной коррозии и скорость коррозии. Вы можете перетащить результат подгонки на график.
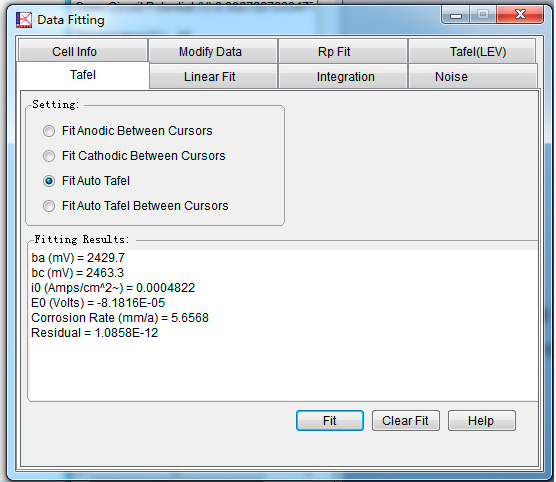
Измерение электрохимического импеданса
Experiments → Impedance → EIS vs. Frequency
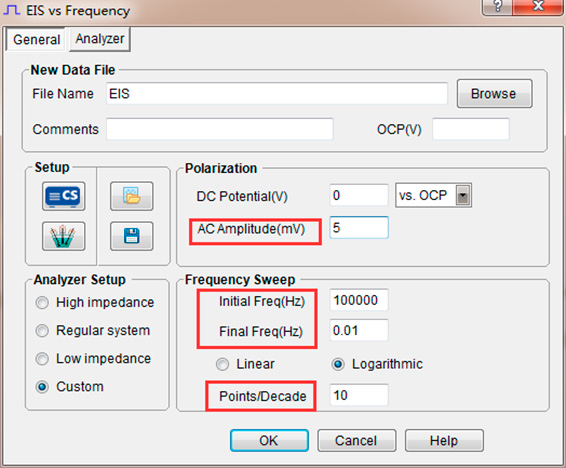
Анализ результатов электрохимического импеданса
График электрохимического импеданса углеродистой стали марки Q235 в 3.5% растворе NaCl представлен ниже:
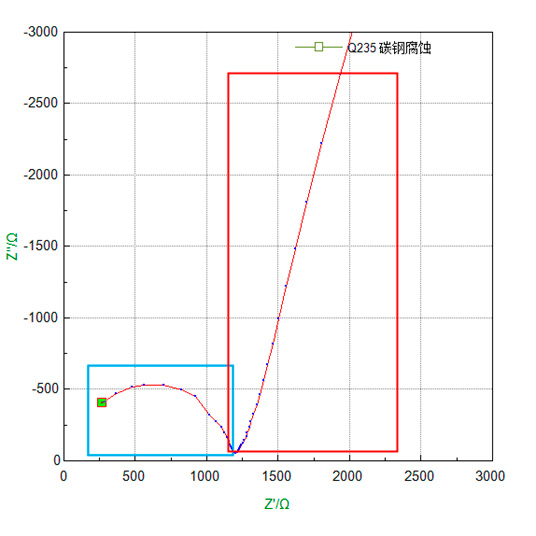 Рисунок 15. Диаграмма Найквисти углеродистой стали Q235.
Рисунок 15. Диаграмма Найквисти углеродистой стали Q235.
Результаты подбора эквивалентной схемы по результам измерения электрохимического импеданса для углеродистой стали Q235
Шаги следующие:
Нарисуйте эквивалентную схему полуокружности – используйте модель в «quick fit», чтобы получить R1, C1, R2.
Нарисуйте эквивалентную схему части импеданса Варбурга — используйте модель в «quick fit», чтобы получить конкретное значение Ws.
Перетащите значения в сложную схему → измените тип всех элементов на «Free+» → нажмите «Подогнать».
Из результатов мы видим, что ошибка составляет менее 5%, что указывает на то, что самостоятельно определяемая нами эквивалентная схема соответствует схеме импеданса фактического измерения. График аппроксимации Боде обычно соответствует исходному графику.
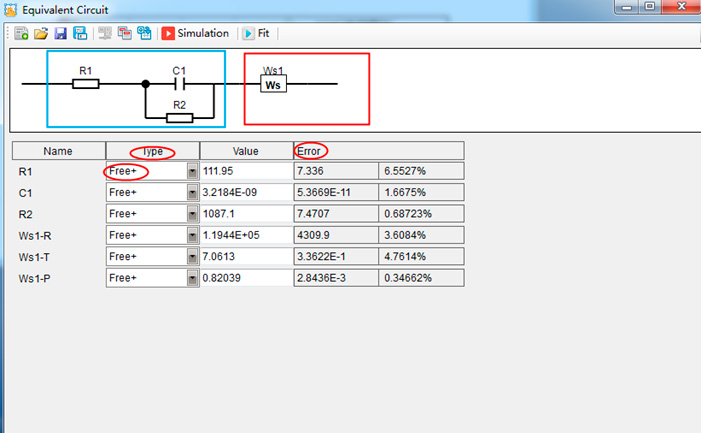
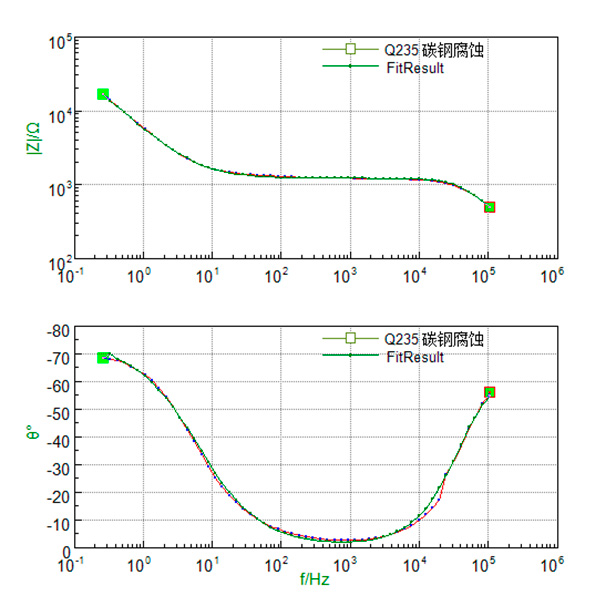 Рисунок 17. Диаграммы Боде Bode: график подгонки и результата фактического измерения.
Рисунок 17. Диаграммы Боде Bode: график подгонки и результата фактического измерения.
Отличия проведения коррозионных испытаний металлов с использованием потенциостата от других испытаний на коррозию
- Скорость: испытания проводятся быстро, можно получить высокую степень коррозии менее чем за час, что контрастирует с испытаниями в камере соляного тумана, которые более затратны по времени.
- Вариация электролита: проведение тестов на потенциостате позволяет выбрать наиболее интересный электролит в любой момент времени, что позволяет воссоздать реальные условия, в которых материал будет работать.
- Небольшой размер образца: в зависимости от используемой электрохимической ячейке, которую имеет потенциостат, испытуемые образцы должны иметь определенный размер, но это обеспечивает гибкость, позволяя проводить измерения от пластин в несколько сантиметров до нитей в несколько микрон толщины.
- Повторяемость: в отличие от других испытаний на коррозию, в которых условия окружающей среды играют важную роль, в испытаниях с потенциостатом влияют только электрические свойства и степени окисления материалов, что дает возможность повторить измерения в любое время и получить те же результаты.
- Количественная оценка: многие испытания на коррозию оцениваются визуально, качественно наблюдая за коррозией, которая проявляется на деталях. Однако испытание потенциостатом позволяет получить числовые значения, которые используются для количественного сравнения свойств материалов и их устойчивости к коррозии.
Связанные публикации в Базе знаний, FAQ и Загрузка:



