Стремительное развитие электроэнергетики во всем мире создает дополнительную нагрузку на производство аккумуляторов. Производство стандартной литий-ионной батареи ограниченно содержанием необходимых минералов и металлов в окружающем мире, поэтому срочно необходимы альтернативы. Литий-серные аккумуляторы представляют собой многообещающее направление в развитии энергетических накопителей. Они обладают рядом уникальных характеристик, которые делают их привлекательными для широкого спектра приложений. Не в последнюю очередь — неограниченная доступность материалов для производства (сера — 16-й по распространенности элемент на Земле) и ее (серы) токсикологическая безопасность при использовании в качестве активного вещества.
Литий-серные аккумуляторы: Принцип работы
Литий-серные аккмуляторы (Li-S) являются родственными литий-ионным аккумуляторам, но существенно отличаются по конструкции и химическим процессам. В этом типе литиевых аккумуляторов используется в качестве положительного электрода сера, а металлический литий — в качестве отрицательного электрода. Литий-серный элемент основан на обратимом преобразовании лития с помощью серы по следующему принципу:
реакция на аноде: 16Li ---- 16Li+ + 16e−
реакция на катоде: S8 + 16e− ---- 8S2-
общая реакция: 16Li + S8 ---- 8Li2S (Eo = 2.24 В)
Теоретический потенциал аккумулятора рассчитывается как E° = 2.24 В, исходя из энтальпии реакции (ΔrG° (при 25°C) = -432.57 кДж/моль [Li2S]). В сочетании с теоретической емкостью 1167 мАч/г (Li2S), результирующая теоретическая плотность энергии составляет 2613 Втч/кг (Li2S). Это значение в несколько раз выше, чем у обычных систем. В литературе часто описывается катодная реакция сама по себе, поэтому указанная там емкость обычно относится к сере. Она составляет 1672 мАч/г (S).
На рис. 1 показана принципиальная схема литий-серного аккумулятора. Необходимо создать подходящую конструкцию катода, поскольку ни сера, ни продукты реакции разряда не являются электропроводящими. В качестве материала-носителя, как правило, используются пористые частицы углерода с большой поверхностью. Они обеспечивают электрический контакт, а также достаточный доступ электролита. Для реакций в акуумуляторехарактерны значительные изменения объема. Li2 (ρ = 1.66 г/см3, Vm = 28,0 мл/моль) имеет меньшую плотность, чем сера (ρ = 2.07 г/см3, Vm = 15,5 мл/моль). Следовательно, на катоде должно быть достаточно места, чтобы компенсировать увеличение объема примерно на 80%. Как правило, катод из серы содержит от 50 до 70% серы по весу. Оставшаяся масса распределяется между углеродосодержащим материалом и связующим веществом (небольшое количество). Углерод также необходимо добавлять к стандартным катодным материалам в качестве проводящей добавки, но в меньшем процентном соотношении. Удельная энергия литий-серного элемента, достижимая на практике, намного ниже теоретической. В основном это связано с высоким содержанием углерода и требуемой высокой пористостью.
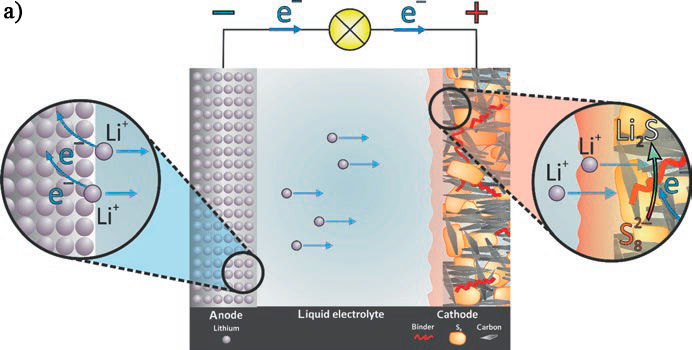

Рисунок 1. а) принципиальная схема литий-серного аккумулятора. Анодным материалом является металлический литий. Катод состоит из смеси частиц серы и углерода, которая механически стабилизируется с помощью связующего вещества. b) Кривые заряда/разряда литий-серного элемента. В начале реакции на катоде из серы и лития образуются растворимые полисульфиды. Они диффундируют к литиевому аноду.
На первый взгляд, реакция, лежащая в основе действия литий-серного аккумулятора, кажется довольно простой, однако при ближайшем рассмотрении она становится очень сложной. Несколько промежуточных стадий восстановления серы до сульфид-иона (S2-) выглядят следующим образом (рис. 2):
В отличие от стандартных растворителей на основе карбонатов, таких как этиленкарбонат (EC) / диметилкарбонат (DMC) с проводящей солью LiPF6 для Li-ion аккумуляторов, литий-серный элемент Li/S8, как правило, содержит смесь диметоксиэтана (DME, C4H10O2), 1.3-диоксолана (DOL, C3H6O2) и бис(трифторметилсульфонил)имид лития (LiN(SO2CF3)2, LiTFSI), поскольку эта смесь наилучшим образом совместима с металлическими литиевыми анодами.

Рисунок 2.
Большинство полисульфидов очень хорошо растворяются в электролите, поэтому механизм реакции значительно отличается от механизма реакции в обычных литий-ионных аккумуляторах, где реакции протекают в твердом состоянии. На рис. 3 наглядно показана растворимость полисульфида в электролите. Электролит приобретает цвет сразу после начала реакции разряда из-за растворенных частиц.

Рисунок 3. Первый разряд литий-серного аккумулятора. На первой стадии реакции на катоде из серы и лития образуются растворимые полисульфиды. Затем они диффундируют к литиевому аноду
До сих пор нет четкого понимания, какие виды частиц появляются, как быстро протекают отдельные частичные реакции и насколько высоки соответствующие концентрации в определенный момент времени. Влияние образования полисульфидов на реакцию ячейки напрямую коррелирует с циклом разряда ячейки (рис. 1 б). Процесс разряда можно разделить на три области. 1 этап: реакция разряда начинается с восстановления элементарной серы S8. Образуются полисульфиды, такие как Li2S8 и Li2S6. Они растворяются в электролите, что приводит к постоянному снижению потенциала при разряда. Минимум характеризует переход в область 2. Причиной является начальное образование твердой фазы Li2S (Li2S2). Требуемая энтальпия нуклеации приводит к дополнительному перенапряжению и, как следствие, к минимуму потенциала цикла разрядка. В зоне 2 продолжается снижение содержания серы. В идеале, полный переход от Li2S2 к Li2S происходит в конце разряда. Однако в аккумуляторах этого обычно не достигается. В целом достигается от 2/3 до 3/4 теоретической емкости. Причинами этого могут быть: недостаточно быстрая диффузия в твердом состоянии при переходе от Li2S2 к Li2S, низкая электропроводность при переходе от Li2S2 к Li2S, блокирование пористого электрода растущими частицами Li2S. Реакция в литий-серном аккумуляторе является сложной и имеет два этапа развития. Следовательно, средний регистрируемый потенциал элемента, составляющий около 2.15 В, ниже расчетного термодинамического значения 2.24 В для прямого перехода от лития и серы к Li2S.
Подходы для долгосрочной стабилизации
В настоящее время тестируется несколько подходов для улучшения характеристик циклируемости литий-серных аккумуляторов. Эти подходы касаются катода (углерод/сера), электролита и анода (металлический литий). Целью, в частности, является ограничение потери активной массы, сохранение механической стабильности катодных конструкций в течение более длительного периода времени. Поэтому для изготовления катода используются специальные углеродные материалы с определенной пористостью (активированный уголь, технический углерод, графен и углеродные нанотрубки). Они обеспечивают достаточный электрический контакт у серы, а также иммобилизуют полисульфидные соединения, чтобы ограничить их потерю в электролите.
В настоящее время для обеспечения достаточной стабильности цикла по-прежнему требуется большое количество электролита и лития. Однако эти меры не позволяют создать батарею с высокой плотностью заряда. Поэтому необходим сбалансированный подход к улучшению отдельных параметров и снижению энергопотребления.
Другой подход заключается в предотвращении диффузии полисульфидных соединений к аноду и паразитное их восстановление. В качестве барьеров используются твердые или гелеобразные полимерные электролиты. Однако по сравнению с жидкими электролитами этот материал обладает меньшей проводимостью и способностью к контакту, что приводит к более высоким перенапряжениям и, следовательно, к снижению энергоэффективности элемента.
Преимущества литий-серных аккумуляторов
- высокая энергетическая плотность. Li-S аккумуляторы обладают одной из самых высоких плотностей энергии среди всех типов аккумуляторов. Это означает, что они способны хранить больше энергии на единицу массы, чем многие другие аккумуляторные технологии.
- долгий срок службы. Это связано с их способностью переносить большое количество циклов заряда и разряда без существенной потери емкости. Они также более устойчивы к проблемам, связанным с образованием "памяти" (эффект потери емкости после неполного разряда).
- хорошая устойчивость к температурным условиям. Li-S аккумуляторы способны работать стабильно при низких температурах, что делает их подходящими для применения в различных сферах, в том числе в космосе и авиации.
- низкая токсичность и экологическая безопасность. По сравнению с некоторыми другими типами аккумуляторов, Li-S батареи считаются менее токсичными и более экологически дружелюбными, так как они не содержат тяжелых металлов, таких как кобальт.
Недостатки литий-серных аккумуляторов
- проблемы с циклируемостью и саморазрядом. После многократных циклов заряда и разряда они могут терять емкость, что ограничивает их срок службы. Кроме того, Li-S аккумуляторы имеют высокий уровень саморазряда, что означает, что они могут разряжаться даже при отсутствии использования.
- проблемы с образованием отложений. В процессе циклов заряда и разряда на аноде могут образовываться лишние отложения лития, что снижает производительность батареи и может вызвать короткое замыкание.
- необходимость усовершенствований. Технология Li-S аккумуляторов все еще находится на этапе активного исследования и разработки.
- ограничения в температурных условиях. Хотя Li-S аккумуляторы обладают хорошей работоспособностью при низких температурах, при высоких температурах они могут сталкиваться с проблемами, такими как образование газов и термическое разложение.
Сравнение Li-S аккумуляторов с другими видами аккумуляторов
|
Параметр |
Li-ion |
Li-Pol |
Li-S |
Ni-Cd |
Ni-MH |
Pb-Acid |
|
Плотность энергии (Втч/кг) |
Высокая |
Очень высокая |
Высокая |
Низкая |
Средняя |
Низкая |
|
Срок службы (циклы) |
300 - 1000+ |
300 - 1000+ |
Перспективно высокий |
1000+ |
300 - 500+ |
200 - 800+ |
|
Саморазряд (в месяц) |
Низкий |
Низкий |
Средний |
Высокий |
Высокий |
Высокий |
|
Эффект памяти |
Нет |
Нет |
Нет |
Да |
Да |
Да |
|
Экологическая безопасность |
Высокая |
Высокая |
Высокая |
Средняя |
Средняя |
Низкая |
|
Рабочая температура (°C) |
-20 — +60 |
-20 — +60 |
-20 — +60 |
-20 — +60 |
-20 — +60 |
-20 — +50 |
Ссылки:
- Chen, Y., et al. (2021). Advances in Lithium-Sulfur Batteries: From Academic Research to Commercial Viability. Advanced Materials, 33, e2003666.
- Zhao, M., et al. (2020). A Perspective toward Practical Lithium-Sulfur Batteries. ACS Central Science, 6, pp.1095-1104.
- Dorfler, S., et al. (2021). Recent Progress and Emerging Application Areas for Lithium-Sulfur Battery Technology. Energy Technology (Weinh), 9, 2000694.



