Содержание:
Слоистые оксиды (LiМО2; М = Co, Ni, Mn, Al)
Шпинели (LiM2O4; M = Mn, Ni)
Фосфаты (LiMPO4; M = Fe, Mn, Co, Ni)
Сравнительные характеристики катодных материалов для ЛИА
Сравнительная оценка достоинств и недостатков основных катодных материалов ЛИА
Заключение
Основным фактором, определяющим ёмкость, мощность и цену литий-ионных аккумуляторов, является материал катода. Размер частиц и площадь поверхности катодного материала определяют сопротивление твердофазной диффузии и реакции переноса заряда положительного электрода литий-ионной батареи. Таким образом, для создания аккумулятора, способного работать на высоких токах, необходимо уменьшение размеров кристаллов активного материала. В качестве катодных материалов используются соединения переходных металлов лития. Эти композиты могут образовывать смешанные кристаллы в широком диапазоне составов.
Основные требования, предъявляемые к катодным материалам:
- химическая устойчивость;
- нерастворимость в электролите;
- низкий химический эквивалент;
- электропроводность.
Далее описаны наиболее важные катодные материалы, их структура и электрохимические характеристики, а также их преимущества и недостатки. Материалы были сгруппированы в три класса в зависимости от их кристаллическая структуры: слоистые оксиды, шпинели и фосфаты.
Слоистые оксиды (LiМО2; М = Co, Ni, Mn, Al)
Наиболее часто изучаемая система катодных материалов состоит из слоистых оксидов с химической формулой LiMO2 (где, M = Co и/или Ni и/или Mn и/или Al). Здесь мы кратко раммотри граничные фазы системы, важные бинарные соединения и наиболее известну тройную фазу Li1−x(Ni0,33Mn0,33Co0,33)O2 (NCM).
Оксид лития-кобальта (Li1-xCoO2, LCO), вероятно, был наиболее широко используемым катодным материалом с момента запуска на рынок первой перезаряжаемой литий-ионной батареи Sony в 1991 году. Li1-xCoO2 имеет структуру α-NaFeO2 (R-3m). В этой структуре кобальт заполняет позиции 3a, а литий — позиции 3b. Оба октаэдрически окружены кислородом в слоях 6c. Два октаэдрических слоя уложены поочередно вдоль оси c (в гексагональной обстановке; вдоль [111] в ромбоэдрической ячейке). Ионы лития в этой структуре могут перемещаться в пределах одной плоскости (2D), перпендикулярной направлению стопки между октаэдрическими слоями кобальта. Следовательно, они могут интеркалировать и деинтеркалировать структуру (Рис. 1).
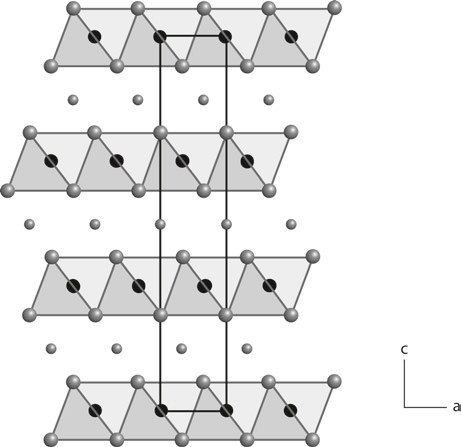
Рисунок 1. Кристаллическая структура Li(1−x)CoO2 (LCO) с выделенной гексагональной элементарной ячейкой (черный Co; серый O; светло-серый Li).
Если литий деинтеркалируется из структуры LCO, образуется окислительно-восстановительная пара Co4+/Co3+, что, в свою очередь, дает потенциал около 4.0 В vs Li/Li+. Почти все ионы лития извлекаются из структуры электрохимически, в результате чего теоретическая емкость составляет 274 мАч/г. Из-за нестабильности фазы с низким содержанием лития (Li1–xCoO2 где x < 0,7) напряжение заряда ограничено величиной ≤ 4.2 В vs Li/Li+ в рабочем диапазоне напряжений. Это означает, что можно использовать лишь немногим более половины доступного лития. Таким образом, максимальная обратимая емкость составляет 140 ÷1 50 мАч/г. Li1–xCoO2 имеет плоскую зарядно-разрядную кривую при рабочем напряжении 3.9 В и наименьшем известном диапазоне рабочих напряжений 0.1 В для обычных интеркаляционных связей лития. Из-за высокого рабочего напряжения, высокой относительной плотности (5.1 г/см3) и насыпной плотности (> 2,2 г/см3) плотность энергии LCO вряд ли может сравниться с другими катодными материалами. Эти аспекты менее важны для приложений с неограниченным пространством, например, для стационарных накопителей энергии, где важны такие критерии, как стабильность и безопасность. Хотя LCO и успешен, это не лучший катодный материал, особенно с точки зрения таких критериев, как безопасность и стабильность. Кислород не может выйти из ячейки и в сочетании с органическим электролитом может бурно реагировать, вызывая пламя или даже взрыв. Кроме того, доказанная растворимость кобальта в обычно используемых электролитах может вызвать растворение ионов кобальта из структуры LCO и привести к потере емкости и, в конечном итоге, к выходу из строя элемента.
Замена всего кобальта в структуре на более дешевый никель приводит к получению оксида лития никеля (Li1–xNiO2, LNO). Хотя LNO имеет ту же структуру, он обладает более высокой обратимой емкостью - около 200 мА/г. При производстве этого соединения в литиевых позициях образуется смешанное заселение около 12% литиевых положений. Вот почему структуру LNO лучше описать как Li1–x–yNi1+yO2. Такое смешанное заполнение вызвано одинаковыми ионными радиусами Li+ и Ni2+, а также нестабильностью Ni3+, что приводит к предпочтению Ni2+ в литированном материале. Доступное количество лития в структуре уменьшается во время разряда из-за смешанного распределения Ni2+ на слоях Li+. Это приводит к необратимой потере емкости материала. Синтез и контроль его параметров имеют первостепенное значение для минимизации беспорядка. Аналогично LCO, в случае LNO существует риск окисления оксидных ионов из-за положения окислительно–восстановительной пары Ni4+/Ni3+ в зонной структуре по сравнению с 2p-состояниями O2-. Это может привести к вышеупомянутым проблемам со стабильностью и безопасностью, вызванным выделением кислорода.
Никель был частично заменен кобальтом до степени замещения < 20%, чтобы устранить негативное воздействие соединения никеля без потери его положительных свойств. Полученные соединения в литированной форме всегда имеют структуру, аналогичную α-NaFeO2. Замена кобальта приводит к уменьшению смешанной нагрузки на слой лития и, следовательно, к повышению обратимой емкости. Кроме того, введение кобальта увеличивает проводимость литий-ионов, а также концентрацию носителей заряда, что повышает электропроводность.
Были использованы дополнительные модификации для повышения стабильности для уменьшения содержания 2р-кислородных полос в зонной структуре, тем самым выводя их за пределы диапазона уровней Ферми, чтобы свести к минимуму выделение кислорода. Одним из способов достижения этой цели является введение алюминия в структуру. Соединение LiNi0.8Co0.15Al0.05O2 (оксид лития никеля кобальта алюминия; NCA) доступно в продаже и, в отличие от LNO, обладает лучшей стабильностью и способностью к циклированию. Частичная замена слоя O2 на F– и S2– соответственно может еще больше повысить стабильность циклирования, поскольку предотвращает миграцию Ni2+ в положение Li+
Соединение Li1–xMnO2 было бы чрезвычайно интересным с экономической и экологической точек зрения. Для такого соединения доступны две возможные фазы. Они значительно различаются по своей электрохимической активности. Термодинамически стабильная ромбическая форма имеет очень неблагоприятные электрохимические характеристики. Электрохимически активную форму (типа α-NaFeO2) трудно синтезировать, поскольку она не является предпочтительной с термодинамической точки зрения. В процессе делитирования Li1–xMnO2 претерпевает фазовое превращение, при котором его состав приблизительно описывается как Li0.5MnO2. В этом диапазоне структура α-NaFeO2 трансформируется в более стабильную шпинельную фазу LiMn2O4. Это фазовое превращение сопровождается уменьшением профиля напряжения.
Концепция создания смешанных кристаллов слоистых оксидов металлов (что приводит к замене положительных характеристик одного иона отрицательными характеристиками другого) привела к разработке оксидов лития, никеля и марганца Li1–x(Ni0.5Mn0.5)O2. Оксид лития никеля марганца обладает самой высокой емкостью среди материалов-аналогов LCO (до 200 мАч/г), несмотря на низкую плотность тока. Степень окисления никеля в этом соединении составляет +2, а марганца - +4. Поскольку напряжение может генерироваться только окислительно-восстановительными парами Ni3+/Ni2+ и Ni4+/Ni3+, полоса 2p-кислорода больше не находится в диапазоне уровня Ферми. По сравнению с NCA, это обеспечивает более стабильное соединение с меньшим выделением кислорода во время зарядки. Ионы никеля стабилизируют структуру α-NaFeO2. В результате во время разряда для оксида лития никеля марганца не наблюдается ни структурного искажения по Ян-Теллеру, ни фазового превращения в шпинельную структуру. Однако, как и в случае с другими соединениями никеля, в позиции лития (позиция 3b) наблюдается смешанное содержание никеля. Для этого соединения оно составляет от 8 до 10 %. Такое смешанное содержание препятствует диффузии лития и, таким образом, снижает обратимую емкость. Включение кобальта в слои 3a может свести к минимуму смешанное использование литиевых элементов, но не может полностью предотвратить это.
Коммерчески очень успешным катодным материалом со слоистой структурой является Li1–x(Ni0.33Mn0.33Co0.33)O2 (оксид лития никеля марганца кобальта, NCM). Это соединение аналогично соединению, получаемому из всех других слоистых оксидов, а именно типа α-NaFeO2. В литированном состоянии металлы имеют заряды Ni2+, Mn4+ и Co3+. Из соображений стабильности структуры не весь литий может быть удален из структуры в NCM. Это также аналогично другим соединениям этого класса. NCM (теоретическая емкость 274 мАч/г) использует только около 66 % имеющегося в конструкции лития и, следовательно, имеет весовую емкость до 160 мАч/г (Рис. 2).
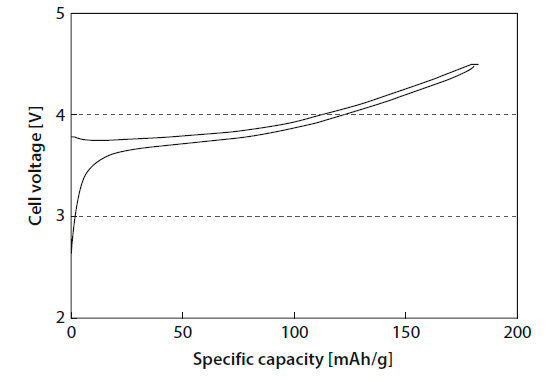
Рисунок 2. Типичный цикл заряда/разряда Li1–x(Ni0.33Mn0.33Co0.33)O2 (NCM) vs Li/Li+.
В диапазоне 0 ≤ x ≤ 1/3 кривая напряжения определяется окислительно-восстановительной парой Ni3+/Ni2+, в диапазоне 1/3 ≤ x ≤ 2/3 - Ni4+/Ni3+, а в диапазоне 2/3 ≤ x ≤ 1 - Co4+/Co3+. В NCM содержание лития и никеля ниже, чем в Li1–x(NiyMn1–y)O2. Это объясняется тем, что он содержит кобальт. Кроме того, кобальт способствует хорошей электропроводности и, следовательно, лучшим электрохимическим характеристикам. Из-за своей степени окисления +4 марганец отрицательно влияет на концентрацию носителей заряда и, следовательно, на электропроводность. С другой стороны, это стабилизирует решетку и, таким образом, повышает устойчивость. По сравнению с граничными фазами системы (LCO, LMO и LNO) взаимодействие выбранных ионов металлов и баланс их преимуществ и недостатков делают NCM материалом с более высокой обратимой способностью и лучшей стабильностью при циклировании.
Тем не менее, у NCM есть недостатки, которые еще не устранены, что оставляет возможности для небольших улучшений. Например, несмотря на десятилетия интенсивных исследований, материалы NCM по-прежнему обладают чрезмерно высокой необратимой емкостью из-за смешанного содержания лития. Кроме того, в измельченном материале могут происходить фазовые превращения. Во время загрузки NCM выделяет кислород. Это было исправлено путем введения алюминия в структуру NCA.
Другой проблемой является напряжение разряда (для NCM: 3,7 В vs Li/Li+). Это все еще низкое значение по сравнению с LCO (3.9 В vs Li/Li+). Эти недостатки оцениваются по-разному в зависимости от конкретного применения и веса.
Современные подходы направлены на использование соединений с низким содержанием кобальта, содержащих менее 25% кобальта или менее 25% марганца. Использование более дешевых металлов должно снизить затраты и увеличить производительность. Исследования показали, что высокое содержание никеля положительно влияет на емкость, обеспечивая производительность до 190 мАч/г (NCM: 160 мАч/г).
Соединения Li1–xMn2O4 (оксид лития марганца, LMO-шпинель) кристаллизуются по типу шпинели (пространственная группа: Fd-3m), где атомы кислорода образуют плотную кубическую упаковку (ccp) на 32e позициях. Атомы марганца занимают позиции 16d и, следовательно, тетраэдрически координированы шестью ионами кислорода. Ионы лития расположены в позициях 8a и тетраэдрически окружены кислородом. Октаэдры MnO6/3 имеют общие ребра и образуют трехмерную решетку (Рис.3). Позиции 16с, которые октаэдрически окружены кислородом, остаются незанятыми и в сочетании с позициями 8а, занятыми литием, образуют трехмерную решетку, через которую могут диффундировать ионы лития. Ионы лития могут быть включены в состав соединений с высоким содержанием лития, таких как октаэдры Li1+xMn2-yO4.
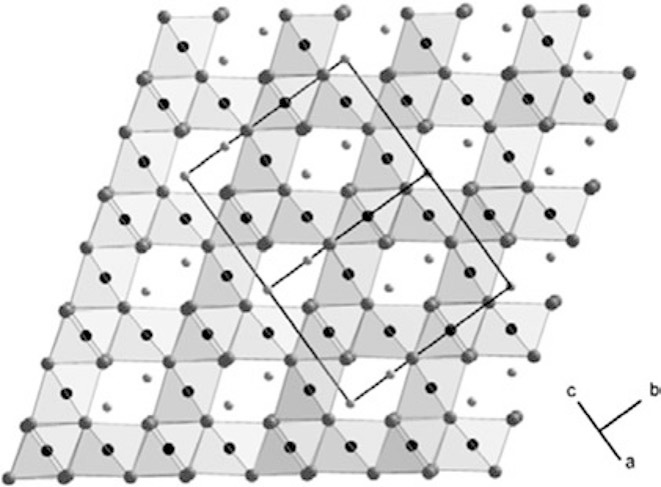
Рисунок 3. Кристаллическая структура LMO-шпинели с выделенной элементарной ячейкой (черный Mn; серый O; светло-серый Li).
Марганец в литированной форме имеет степени окисления +3 и +4. Трехвалентный марганец окисляется в процессе делитирования, и окислительно-восстановительная пара Mn3+/Mn4+ определяет рабочее напряжение в 4.1 В vs Li/Li+ (Рис. 4).
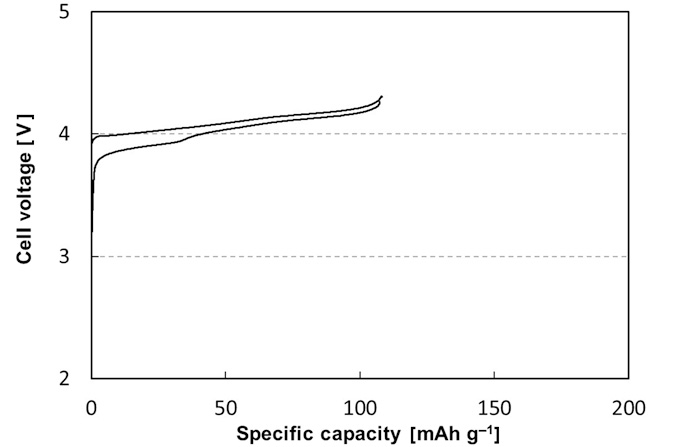
Рисунок 4. Типичные циклы заряда/разряда LMO–шпинели (Li1-xMn2O4 vs Li/Li+).
Li1–xMn2O4 и его варианты легирования, подобно LCO и NCM, являются признанными коммерческими катодными материалами. Их внедрение в качестве катодных материалов первого поколения является результатом многолетних исследований и разработок, направленных на улучшение электрохимических характеристик LMO-шпинели. Среди прочего, на протяжении десятилетий исследователи уделяли особое внимание контролю морфологии и химическому составу поверхности кристаллитов Li1–xMn2O4.
LMO как катодный материал проявляет плохие циклические свойства, что приводит к постоянному снижению обратимой емкости. Эта характеристика еще более выражена при температурах выше 50 °C, что может легко произойти в стационарных и автомобильных установках. Такое поведение может быть вызвано множеством факторов. Вероятно, наиболее важной причиной является неустойчивость Li1–xMn2O4 к кислотам. Например, небольшое количество воды может вступать в реакцию с проводящей солью в результате чего образуется фтористый водород.
Ионы Mn2+, растворенные в ходе электролитической реакции, могут осаждаться на катоде в виде MnO или MnF2. В то же время шпинель материала катода превращается в дефицитную шпинель с высоким содержанием Mn4+ (Li2MnO4 и Li4Mn5O12 соответственно). Отложения MnO на аноде оказывают негативное воздействие на поверхность раздела твердых электролитов (SEI).
Шпинели LMO могут разряжаться при высоких токах (> 5 C). Зарядка LMO большим током ограничена из-за небольшого диапазона зарядных напряжений (0.3 В).
В последнее время исследователи проявляют все больший интерес к LMO-шпинелям с наночастицами и/или наноструктурами. Такие структуры обладают еще большей способностью к разрядке при высоких токах. Наноструктурированные материалы имеют большую поверхность, что делает растворимость Mn3+ важным параметром. Поэтому шпинели из наночастиц LMO в основном имеют покрытие.
Другими весьма интересными материалами для будущих применений являются материалы с более высоким рабочим напряжением (> 4.0 В), в том числе высоковольтные шпинели, такие как Li1x(Ni0.5Mn1.5)O4. Эти высоковольтные шпинели имеют напряжение 4.7 В (vs с Li/Li+), что обеспечивает плотность энергии, которая на 12% выше, чем у коммерчески доступных материалов. Другие высоковольтные шпинели (Li1-x(M0.5Mn1.5)O4 с M = Cr, Co, Fe и Cu) также являются возможными альтернативами. По сравнению с LMO, эти соединения имеют больший диапазон напряжений зарядf и разрядf, а также максимальное рабочее напряжение до 5.1 В vs Li/Li+. Стабильность электролитов в настоящее время является основным препятствием, с которым сталкиваются разработчики высоковольтных материалов. Преобладающие электролиты стабильны примерно до 4.3 В vs Li/Li+, но при превышении этого значения они сами подвергаются электролизу, что снижает циклическую стабильность элемента.
Фосфаты (LiMPO4; M = Fe, Mn, Co, Ni)
LiFePO4 (фосфат железа лития; LFP) был представлен в качестве катодного материала в 1997 году и кристаллизуется подобно природному минералу литиофилиту оливинового типа пространственной группы Pnma (Рис. 5). Атомы кислорода образуют почти идеальную гексагональную плотную упаковку (hcp); атомы лития (слой 4a) и атомы железа (слой 4c) расположены в правильном порядке в октаэдрических пространствах этой упаковки. Пространства тетраэдра содержат атомы фосфора (слой 4с), которые посредством ковалентных связей образуют ион фосфора с четырьмя соседними атомами кислорода и искажают структуру (Рис. 5). Искаженные октаэдрические координационные многогранники лития имеют общие ребра [010] ии образуют одномерный диффузионный путь, параллельный оси b для ионов лития. Внешние электроны ионов кислорода поляризованы в сильно ковалентных связях P-O из-за индуктивного эффекта атомов фосфора, ослабляющего ковалентность связи Fe-O. Это приводит к снижению окислительно-восстановительной энергии окислительно-восстановительной пары Fe3+/Fe2+ и более высокому напряжению холостого хода по сравнению с Li/Li+ (Voc). Этот эффект также наблюдался в других полианионных соединениях литий-железо, но он усиливается структурой оливина для LFP.
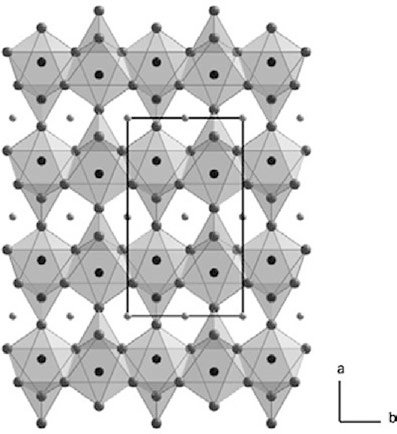
Рисунок 5. Кристаллическая структура LFP с выделенной элементарной ячейкой (крупные шары: черный Fe; серый O; серый P; темно-серый и маленький шар - Li).
Другой характеристикой LFP является его чрезвычайно плоское плато заряда и разряда (Рис. 6), что обусловлено наличием структурно очень похожих граничных фаз. Эти граничные фазы характеризуются незначительными различиями в их кристаллической структуре. Объем фазы с низким содержанием лития всего на 6.81 % меньше, а ее плотность всего на 2.59 % ниже, чем у фазы с высоким содержанием лития.
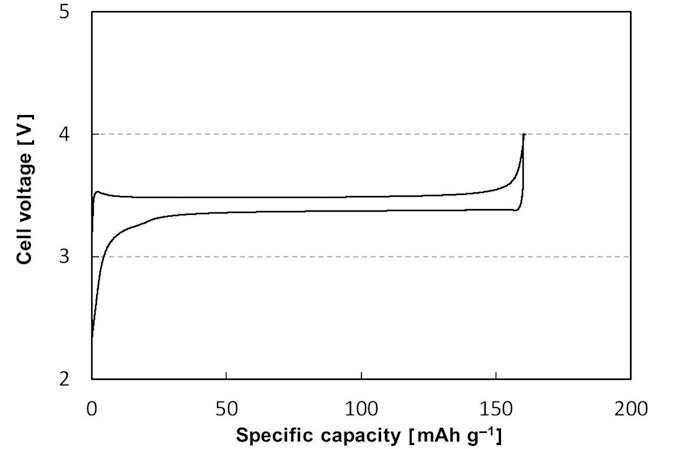
Рисунок 6. Типичные циклы заряда/разряда LFP (Li1-xFePO4 vs Li/Li+).
Таким образом, отсутствуют структурные дефекты или возникающие в результате этого напряжения, которые могли бы повредить материал и снизить стабильность при циклировании. Стабильность делитированной фазы (FePO4) способствует исключительной стабильности лития железа фосфата при циклировании. Обусловленное диффузией разрастание фаз определяет характеристики только при чрезвычайно высоких токах (> 20 C), но при высоких температурах (> 50°C) LFP демонстрирует лучшие характеристики заряда и разряда, чем материалы, рассмотренные выше.
Самой большой проблемой этого материала является плохая электрическая и литий-ионная проводимость. Уменьшение кристаллов катодного материала должно уменьшить расстояние для диффузии литий-ионов, а также уменьшить расстояние, которое электроны должны пройти через материал. Поэтому разработано множество технологий для производства частиц LFP в субмикроном или даже нанометровом диапазоне. Обычно литий-железофосфаты в основном состоят из первичных частиц диаметром ~200 нм, которые агломерируются во вторичные частицы диаметром от 5 до 10 мкм. Уменьшение размера частиц компенсирует литий-ионную проводимость. Однако, он не улучшает электропроводность. Плохая электропроводность катода материала приводит к ухудшению работы батарей. По этой причине проводимость стала одной из ключевых целей исследований LFP. Карбоновое покрытие, например, может значительно улучшить проводимость LFP.
В сравнении с другими материалами катода LFP обладает улучшенной термической и химической стабильностью. Также этому материалу свойственны следующие достоинства:
- безопасность — элементы на основе катодного материала LFP защищены от взрывов и воспламенений, даже при разгерметизации;
- большой рабочий ресурс. Аккумуляторы на основе LFP рассчитаны на долговечную эксплуатацию. Срок их службы достигает от 3 000 до 5 000 рабочих циклов со снижением емкости не более чем на 20 %;
- стабильная работа в температурном диапазоне от -30 °С до +50 °С;
- возможность быстрой зарядки посредством высоких токов;
- меньшая уязвимость к эффекту старения — снижение рабочей емкости у ячеек литий-железо-фосфатных элементов происходит со скоростью 1.5 % в год, тогда ак прочие Li-ion энергоносители имеют степень износа до 10 % за идентичный период;
- отсутствие вредных выделений при работе и разложении, что существенно упрощает процесс их утилизации.
В настоящее время в качестве катодных материалов на основе фосфатов отдают предпочтение смешанным фосфатам железа и марганца. Основные характеристики материалов для ЛИА и их сравнение можно найти в таблицах ниже.
Сравнительные характеристики катодных материалов для ЛИА
|
Параметр/тип |
LiCoO2 |
LiMn2O4 |
LiNiMnCoO2 |
LiFePO4 |
LiNiCoAlO2 |
|
Напряжение элемента, В |
3.6 |
3.7 |
3.6–3.7 |
3.2 |
3.6 |
|
Оптимальная глубина разряда, % |
85–90 |
85–90 |
85–90 |
85–90 |
85–90 |
|
Допустимая глубина разряда, % |
100 |
100 |
100 |
100 |
100 |
|
Циклический ресурс, D.O.D.=80% |
700 ÷ 1000 |
1000 ÷ 2000 |
1000 ÷ 2000 |
1000 ÷ 2000 |
1000 ÷ 2000 |
|
Оптимальная температура, °С |
+20…+30 |
+20…+30 |
+20…+30 |
+20…+30 |
+20…+30 |
|
Диапазон рабочих температур, °С |
–10… +60 |
–10…+45 |
–10…+55 |
–10… +60 |
–10…+55 |
|
Срок службы лет, при +20 °С |
5 ÷ 7 |
10 |
10 |
20 ÷ 25 |
20 ÷ 25 |
|
Саморазряд в мес., % |
1 ÷ 2 |
1 ÷ 2 |
1 ÷ 2 |
1 ÷ 2 |
1 ÷ 2 |
|
Максимальный ток заряда (C - емкость) |
0.7 ÷ 1С |
0.7 ÷ 1С |
0.7 ÷ 1С |
1C |
0.7C |
|
Минимальное время заряда, ч |
2 ÷ 3 |
2 ÷ 2.5 |
2 ÷ 3 |
2 ÷ 3 |
2 ÷ 3 |
|
Уровень стоимости |
высокий |
средний |
средний |
низкий |
средний |
Сравнительная оценка достоинств и недостатков основных катодных материалов ЛИА
|
Материал катода |
Достоинства |
Недостатки |
|
LiCoO2 |
1. Хорошая циклируемость; 2. Термическая стабильность; 3. Отсутствие фазовых переходов; 4. Допирование Co способствует усилению кристалличности и увеличению параметров ячейки. |
1. Высокая стоимость; 2. Невозможность полной деинтеркаляции лития. |
|
LiNiO2 |
1. Высокое рабочее напряжение; 2. Большая удельная ёмкость; 3. Низкая стоимость. |
1. Трудность синтеза LiNiO2 стехиометрического состава; 2. Термическая неустойчивость; 3. Структурное разупорядочение; и падение ёмкости при циклировании; 4. Низкая циклируемость. |
|
LiMn2O4 |
1. Недорогой материал; 2. Отсутствие токсичности, отвечает требованиям безопасности; 3. Избыток лития способствует повышению сохранности заряда; 4. Повышенная структурная разупорядоченность способствует структурной стабильности при внедрении добавочных ионов лития, что улучшает циклируемость в области 3 В. |
1. Сильно падает ёмкость после циклирования в интервале от 3 до 4 В. |
|
LiFePO4 |
1. Безопасность и текущий высокий рейтинг при выборе. LiFePO4 является более безопасным катодным материалом, чем LiCoO2; 2. Связь Fe–P–O прочнее, чем Co–O, так что при неправильном обращении (коротком замыкании, перегреве и т. д.) отщепление атомов кислорода происходит гораздо труднее; 3. LiFePO4 остаётся стабильным во время потери кислорода, которая обычно приводит к экзотермическим реакциям в аккумуляторах c другой химией. |
1. Более низкие напряжение и плотность тока, чем у других литий-ионных аккумуляторов. |
Таким образом, слоистые оксиды в качестве катодного материала выгодны в тех случаях, когда требуется высокая результирующая плотность энергии. В литосфере эти металлы очень редки, что приводит к высокой стоимости конечного электродного материала.
Железо — второй по распространенности элемент на земле и очень недорогой. Потому, LFP — это самая дешевая возможность производства 1 кг катодного материала. Почти все оксидные катодные материалы проявляют сильные экзотермические эффекты, что может привести к воспламенению и взрыву ячейки. Риск такого развития событий практически отсутствует для LFP. Кроме того, LFP и LFMP нетоксичны для окружающей среды. Это не относится к оксидным соединениям, содержащим тяжелые металлы.
Диффузия лития возможна в одном направлении в случае катодного материала LFP, тогда как другие материалы имеют двумерные, если не даже трехмерные пути диффузии лития. Тем не менее, LFP — единственный катодный материал, который можно быстро заряжать и разряжать.
Оксиды были в центре внимания исследований и разработок с восьмидесятых годов. Их много раз модифицировали, в результате чего появились материалы, которые можно производить в больших объемах. Развитие относительно «молодых» катодных материалов на основе фосфатов все еще находятся в зачаточном состоянии. С ними возможно достичь более высоких рабочих напряжений с более высокой плотностью энергии за счет замены железа на марганец, кобальт или никель. Это делает соединения на основе фосфатов перспективными катодными материалами для будущих приложений высокого напряжения.



