Литий-ионный аккумулятор (ЛИА), как следует из названия, представляет собой тип перезаряжаемой батареи, которая накапливает и разряжает энергию за счет движения ионов лития между двумя электродами с противоположной полярностью, называемыми катодом и анодом, через электролит. Это непрерывное перемещение ионов лития от анода к катоду и наоборот имеет решающее значение для функционирования литий-ионного аккумулятора. Анод, также известный как отрицательно заряженный электрод, выделяет ионы лития в электролит. Выделяющиеся ионы затем направляются к катоду, который также называют положительно заряженным электродом, где они поглощаются. Это, в простом изложении, и есть процесс выделения энергии в ЛИА.
Идеальный анод должен отвечать следующим условиям:
- содержать элементы со сравнительно низкой атомной массой и способностью к внедрению большого количества лития;
- иметь рабочий потенциал, как можно более близкий к рабочему потенциалу металлического лития;
- не должен растворяться или взаимодействовать с растворителем и солевым компонентом электролита;
- иметь хорошую обратимость реакций заряда и разряда;
- обладать размерной и механической инвариантностью в процессе интеркаляции/деинтеркаляции лития.
Введение
Вторичные литиевые элементы изначально имели металлическую литиевую фольгу в качестве анода (отрицательный электрод) [1]. Чистый литий имеет очень высокую удельную емкость (3860 мАч/г) и очень отрицательный потенциал, что приводит к очень высокому напряжению элемента. Однако эффективность элемента при длительном циклирования снижается, поскольку литий постоянно растворяется во время разряда элемента и осаждается во время его заряда. Это означает, что его необходимо использовать в двух и даже трех раз избыточное количество. Кроме того, литий может осаждаться в виде пены и в виде дендритов. Последние могут прорастать через сепаратор [2, 3]. Эти дендриты могут вызывать локальные короткие замыкания, что может привести к полной саморазрядке элемента или, в худшем случае, к внутренней тепловой цепной реакции, возгоранию или взрыву.
В настоящее время с литиевым анодом массово производятся только небольшие элементы (как правило, монетного типоразмера). Благодаря металлическим литиевым анодам к ним предъявляются низкие требования в отношении стабильности работы и возможности быстрого заряда. Однако недавно были возобновлены испытания элементов большой емкости. В этих испытаниях используются специальные сепараторы (см. Bolloré [4]). Наиболее важными аспектами для этих литий-металлополимерных элементов по-прежнему остаются безопасность и стабильность работы.
Для получения безопасных элементов с хорошей эффективностью циклирования металлический литий заменяют так называемым литиевым интеркаляционным материалом [5-8]. Как правило, процесс интеркаляции, например, в углерод, является обратимым процессом без потерь, и образования литиевого покрытия не происходит [9, 10]. Литий-ионные аккумуляторы, типичные для рынка “Электроника 3C” (портативные бытовые устройства), оснащены анодами из графита. Поэтому, все большее внимание уделяется использованию аморфных углеродов (hard и soft углеродов) в новых областях применения, которые обеспечивают более высокую мощность и плотность энергии, а также повышенную безопасность. Отчасти, они обладают лучшей проводимостью по току и являются более безопасными и стабильными в сочетании с новыми электролитами и катодными материалами.
Их емкость запаса лития намного выше, чем у графита, благодаря использованию металлов и сплавов (интерметаллических соединений), которые могут обратимо реагировать с литием. Системы на основе металлов пока не производятся массово, несмотря на интенсивные усилия в области НИОКР. Поэтому все еще существует значительная потребность в исследованиях. Даже если добавление углерода (например, композит C/Si, композит C/Sn) позволяет их улучшить, то стабильность при циклировании остается недостаточной. Титанат лития и оксид титана являются перспективными в качестве активных анодных материалов для улучшения стабильности при циклировании и отвечают чрезвычайно высоким требованиям мощности и безопасности. Однако удельная емкость этих материалов очень низкая, а потенциал vs лития является очень высоким (рис. 1).
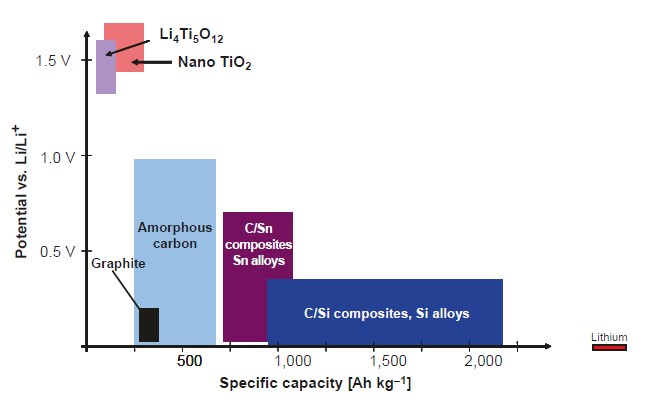 Рисунок 1. Удельная емкость и потенциал vs Li/Li+ наиболее важных анодных материалов [11].
Рисунок 1. Удельная емкость и потенциал vs Li/Li+ наиболее важных анодных материалов [11].
Электрохимические характеристики этих материалов играют важную роль. Кроме того, хорошая обрабатываемость (реологические характеристики, адгезия к металлической фольге и т. д.) является обязательным условием при производстве электродов. На рис. 5.1 представлен обзор удельной емкости и потенциала наиболее важных анодных материалов [11]. В следующих разделах будет предоставлена информация о различных анодных материалах.
Производство и структура аморфных углерода и графита
Как аморфный углерод (hard и soft углерод), так и графит встречаются в природе, так же возможен их синтез. Типичным представителем природного аморфного углерода является антрацит. Природный графит называется natural graphite. Крупнейшие месторождения природного графита находятся в Азии, в основном в Китае. Также есть месторождения в Индии и Северной Корее. В Западном полушарии природный графит в основном добывают в Бразилии и Канаде. Предполагается, что около 70–80 % всего природного графита залегает в Китае. По этой причине в 2010 году Инициатива Европейского союза по сырьевым материалам включила природный графит в свой список из 14 критически важных видов сырья. Природный графит необходимо отделить от рудного вещества, чтобы сделать его пригодным для использования в аккумуляторах. Он также должен быть очищен химическим, термическим и/или обоими способами.
Исходными материалами для синтеза аморфного углерода и графита обычно являются побочные продукты угольной и нефтяной промышленности. В последнем случае наиболее распространенными материалами являются нефтяной кокс и смолы с высоким содержанием ароматических соединений, например, фенольные смолы. В угольной промышленности наиболее важным сырьем являются каменноугольный пек и высокоизотропный кокс. Исходные материалы карбонизуются или прокаливаются при низких температурах (от 800 °C до 1200 °C). Первым продуктом является аморфный углерод. Если карбонизированный исходный материал (например, фурановая смола или фенольная смола) остается аморфным при последующей термообработке при температуре до 3000°C, его называют твердым или неграфитизируемым углеродом. Если карбонизированный исходный материал (например, кокс или пек) превращается в графит выше 2500 °C, его называют мягким или графитизируемым углеродом.
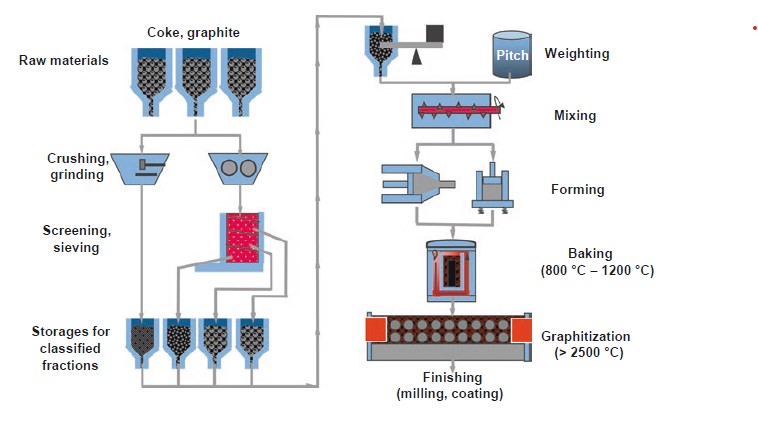 Рисунок 2. Принципиальная схема производства синтетического графита.
Рисунок 2. Принципиальная схема производства синтетического графита.
На рис. 2 представлен обзор типичного процесса производства синтетического графита. Основным сырьем являются прокаленный кокс в качестве твердого материала и каменноугольный пек в качестве связующего. Твердые материалы проходят предварительную обработку (измельчаются, просеиваются, сортируются по сортам). Затем материал смешивается с расплавленным жидким связующим пеком для получения пластифицированной сырой массы, которая впоследствии формуется, например, экструзией или компрессионным формованием.
Затем затвердевшую сырую массу подвергают обжигу при температуре от 800°C до 1200°C в отсутствие кислорода. Смола карбонизируется, образуя аморфный углерод в качестве связующей фазы. Чтобы превратить аморфный углерод в синтетический графит, массу помещают в так называемый карбонизатор и обрабатывают при температуре >2500 °C. Современные технологии графитации восходят к Ачесону или Кастнеру [12, 13] и были изобретены в конце 19 века. Типичное количество электроэнергии, необходимое для производства 1 кг графита в печи Ачесона, составляет от 3 до 4 кВт·ч, а необходимое время работы печи составляет около трех недель. Высокие температуры приводят к удалению загрязнений из графита, и образуется типичная структура графитового слоя (рис. 3 а и b). Графит является одним из самых известных аллотропных модификаций углерода. Он состоит из параллельно уложенных слоев графена. Графен представляет собой гексагональную решетку из sp2-гибридизованных атомов углерода. Широко распространенная гексагональная форма графита имеет последовательность слоев ABABAB (рис. 3 b). Расстояние между слоями графена составляет 0.3354 нм.
Ромбоэдрическая модификация графита с последовательностью слоев ABCABC имеет меньшее значение; ее процентное содержание может достигать 20 % от массы во время процессов формования, таких как измельчение графита. Это соотношение можно снова уменьшить с помощью высокотемпературной обработки [15]. Кристаллографическая плотность обеих форм графита составляет 2.26 г/см3.
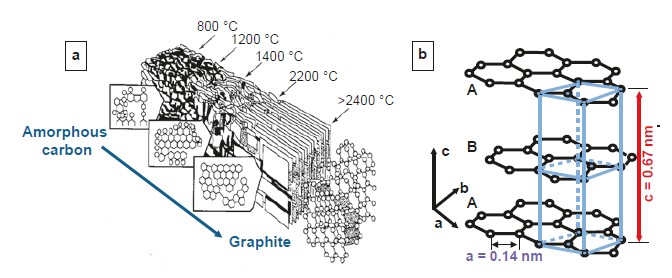 Рисунок 3. (а) Развитие структуры графитового слоя из аморфного, графитизируемого углерода по Маршу [14], (б) гексагональная структура графита.
Рисунок 3. (а) Развитие структуры графитового слоя из аморфного, графитизируемого углерода по Маршу [14], (б) гексагональная структура графита.
Во многих случаях для оптимального использования графита в качестве активного материала в зависимости от области применения применяются дополнительные процессы обработки (рис. 4). Окончательный размер и форма частиц достигается после измельчения графита (рис. 4 а). Это гарантирует, что удельная площадь поверхности будет как можно меньше, а морфология поверхности — как можно более гладкой (морфологии частиц в форме картофеля, рис. 4 b). Исключением в этом отношении являются графиты или мягкие угли на основе мезофазной смолы. При изготовлении они имеют почти круглую форму, поэтому их не нужно подвергать процессу округления в виде порошка после карбонизации или графитизации. Дальнейший процесс обработки графитового порошка включает нанесение на него слоя аморфного или графитового углерода (рис. 4 c). Причины, по которым применяются процессы порошковой обработки (закругление и нанесение покрытия), связаны с электрохимией и будут изложены в следующей главе.
 Рисунок 4. Частицы графита (а) без закругления, (b) округлые, (c) с аморфным углеродным покрытием.
Рисунок 4. Частицы графита (а) без закругления, (b) округлые, (c) с аморфным углеродным покрытием.
Интеркаляция лития в графите и аморфных углеродах
Отрицательный электрод первого коммерческого литий-ионного элемента, выпущенного на рынок Sony Energytec Inc. в 1991 году [1, 15, 16], был изготовлен из hard carbon, который был получен путем карбонизации смолы полифурфурилового спирта (PFA).
Этот успех вызвал рост научно-исследовательской и опытно-конструкторской деятельности в области изучения электрохимических характеристик и процессов интеркаляции аморфного углерода и графита.
Электрохимическая интеркаляция несольватированного лития в графите происходит в диапазоне потенциалов от 0 до 0.25 В vs Li/Li+. Она проходит, с проявлением четко выраженного двухфазного механизма с четко определенными химическими соединениями в начале и конце плато (рис. 5 а). Обе фазы одновременно присутствуют на протяжении всего плато. Эксперименты показали, что этапы интеркаляции поддаются измерению (рис. 5 b и c) и легко различимы благодаря их цвету (рис. 6). Гексагональная (ABABAB) и ромбоэдрическая (ABCABC) структуры графита, соответственно, трансформируются в последовательность стопки AAAAAA с интеркалированным литием во время интеркаляции. Литий располагается в центре колец C6 между двумя графеновыми слоями. Поэтому емкость графита зависит от количества доступных слоев графена. На практике почти возможно достичь теоретической обратимой удельной емкости 372 мАч/г, если использовать очень хорошо структурированный графит (например, природный графит/natural graphite) и медленные скорости заряда (низкие токи заряда).
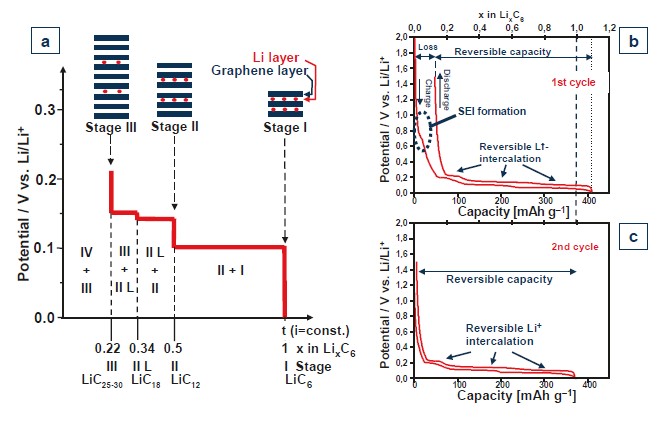 Рисунок 5. (а) Термодинамика интеркаляции лития в графит [17] с фазами: I-LiC6, II-LiC12.II-LiC18, III-LiC25-30, IV–LiC36-50. Гальваностатический цикл заряда и разряда графита с металлическим литием в качестве противоэлектрода и электрода сравнения для первого (b) и второго (c) циклов.
Рисунок 5. (а) Термодинамика интеркаляции лития в графит [17] с фазами: I-LiC6, II-LiC12.II-LiC18, III-LiC25-30, IV–LiC36-50. Гальваностатический цикл заряда и разряда графита с металлическим литием в качестве противоэлектрода и электрода сравнения для первого (b) и второго (c) циклов.
 Рисунок 6. Изображение частично заряженного анода [18].
Рисунок 6. Изображение частично заряженного анода [18].
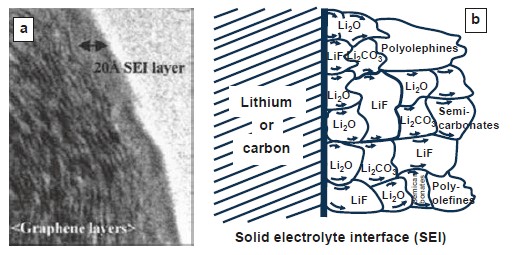 Рисунок 7. (а) Изображение ТЭМ [20] и (b) схематическая диаграмма химического состава SEI [21]
Рисунок 7. (а) Изображение ТЭМ [20] и (b) схематическая диаграмма химического состава SEI [21]
Рис. 5 b показывает, что существует разница между зарядной и разрядной емкостью первого цикла. Эта потеря емкости является результатом электрохимических реакций между ионами лития из катода, компонентами электролита (органические карбонаты, добавки и т. д.) и поверхностью анода.
В результате этой электрохимической реакции между электролитом и частицами графита образуется пассивирующий слой. Этот слой (рис. 7 а, b) называется SEI (межфазный слой твердого электролита) [19]. Качество SEI в значительной степени влияет на стабильность циклирования, срок службы, мощность и безопасность литий-ионных аккумуляторов. Например, SEI должен обладать максимально возможной литий-ионной проводимостью для достижения минимально возможного перенапряжения.
В то же время SEI должен выполнять функцию фильтра для сольватированного литий-ионного растворителя. Это предотвращает совместное проникновение растворителей, которое в противном случае разрушило бы решетку графита. Кроме того, SEI должен хорошо прилипать к частицам анода и быть в определенной степени расширяемым (обеспечивая увеличение объема без растрескивания частиц анода во время интеркаляции), чтобы предотвратить дальнейшие потери при циклировании.
Химия электролита и физические и химические особенности поверхность анода в значительной степени влияют на толщину и химический состав слоя SEI. Наиболее важными характеристиками поверхности анода являются удельная поверхность (в зависимости от формы частиц, размера частиц и пористости) и химия поверхности (например, такие группы, как –COOH, –CO, –OH). Форма частиц, размер частиц и химия поверхности также влияют на стабильность и качество суспензии, которая используется в качестве покрытия для токосъемника (медной фольги) во время изготовления электродов. Круглые частицы лучше текут во время процессов смешивания и нанесения, а также имеют более низкую удельную поверхность. Это означает, что в составе электрода требуется меньше связующего, а для формирования SEI во время первого цикла зарядки используется меньшее количество ионов лития и меньшее количество электролита. Модификация химической поверхности во время окисления/восстановления или на технологических стадиях, таких как нанесение покрытия из частиц графитового анодного материала, оказывает влияние на качество SEI, а также на адгезию к медной фольге и самому SEI. В отличие от графита, аморфные углероды (hard и soft carbon, рис. 8 и 9) не имеют по-настоящему постоянного дальнего порядка. Упорядоченные области чрезвычайно малы, а расстояния между локальными слоями значительно различаются. Внутри материала имеются отчетливые области с кластерами вакансий, гетероатомами и функциональными группами (например, – COOH, – OH). Эти факторы приводят к существенному различию электрохимических характеристик (рис. 8).
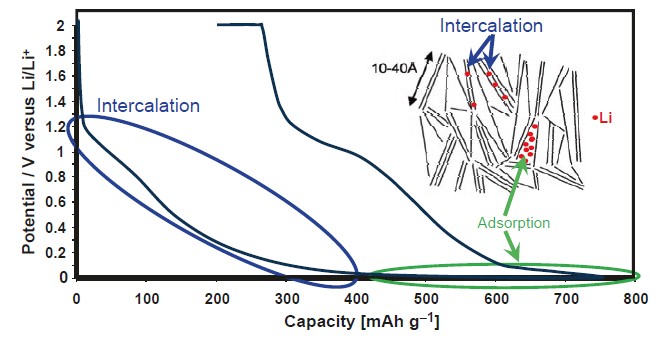 Рисунок 8. Гальваностатическая кривая первого цикла заряда и разряда для аморфных углей с металлическим литием в качестве противоэлектрода и электрода сравнения.
Рисунок 8. Гальваностатическая кривая первого цикла заряда и разряда для аморфных углей с металлическим литием в качестве противоэлектрода и электрода сравнения.
Все аморфные углероды имеют одинаковую структуру и следующие электрохимические характеристики:
- высокая удельная емкость при крайне низких скоростях зарядки, несмотря на низкую степень порядка;
- высокая потеря емкости в течение первого цикла, несмотря на низкую удельную поверхность (BET);
- большой гистерезис гальваностатической кривой для процесса интеркаляции и деинтеркаляции лития.
В отличие от графита, интеркаляция лития в области выраженного ближнего порядка происходит не на определенных этапах, а более или менее непрерывно (рис. 8). Вблизи нулевого напряжения vs Li/Li+ наблюдается дополнительная емкость. Это происходит уже не из-за интеркаляции лития между слоями графена, а из-за адсорбции лития на внутренних поверхностях нанополостей [22-24]. В более крупных порах также возможно размещение кластеров металлического лития. Однако эта дополнительная емкость доступна только при очень низкой скорости заряда (C), поскольку литий должен полностью проникнуть в нанопоры. Как правило, для обеспечения высокой скорости заряда, необходимой для типичных промышленных применений, можно использовать только промежуточную часть. В целом, удельная поверхность BET аморфных углей меньше или близка к таковой графита. Следовательно, можно было бы ожидать аналогичной потери емкости из-за образования SEI во время первого цикла зарядки. Но, как показано на рис. 8, разница между зарядной и разрядной емкостью чрезвычайно велика (здесь: около 200 мАч/г). Чрезвычайно высокая потеря емкости во время первого цикла вызвана сильной реакцией лития с поверхностными дефектами (C-sp3), с гетероатомами, а также функциональными группами на внутренней и внешней поверхностях.
Поскольку для промышленного использования и требуемых скоростей заряда подходит только область интеркаляция, полезная емкость аморфных углей меньше, чем у графита. При очень высоких скоростях зарядки аморфные углероды интегрируют литий гораздо быстрее, чем графит (это показано на рис. 9 а). Эта характеристика также наблюдается при сравнении структур графита и аморфных углей (рис. 9 b). Графит предлагает только несколько «точек входа» для лития (на передних краях областей слоя с большим расстоянием) для входа в решетку, откуда он должен диффундировать в центр дальних кристаллических доменов. Аморфные угли, с другой стороны, предлагают больше точек входа. Распределение лития внутри упорядоченных слоев также очень быстрое, поскольку расстояния диффузии очень короткие. Более того, эти домены с ближним порядком также связаны друг с другом, что снижает тенденцию к расслоению. Таким образом, аморфные углероды демонстрируют лучшую циклическую стабильность с электрохимической точки зрения, особенно при более высоких скоростях заряда (скоростях С).
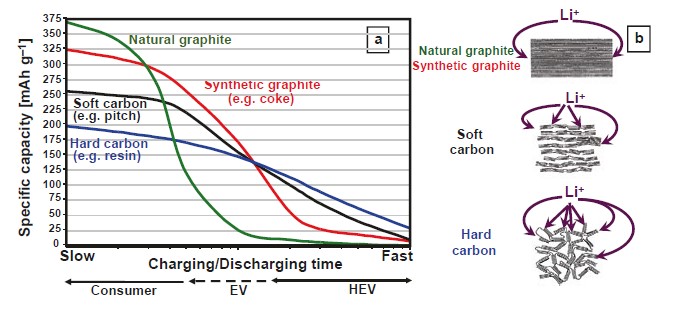 Рисунок 9. (a) Схематическая диаграмма зависимости емкости от скорости заряда и (b) модели интеркаляционной структуры различных анодных материалов на основе углерода. В скобках указано исходное сырье.
Рисунок 9. (a) Схематическая диаграмма зависимости емкости от скорости заряда и (b) модели интеркаляционной структуры различных анодных материалов на основе углерода. В скобках указано исходное сырье.
Производство и электрохимические характеристики композитов C/Si или C/Sn
Как и в случае с графитом, литий внедряется в кремний, проявляя четко определенное двухфазные плато с четко определенными химическими соединениями в начале и конце плато (рис. 10). Состав и соответствующие потенциала vs Li/Li+ [25]: Si/Li12Si7 (332 мВ); Li12Si7/Li7Si3 (288 мВ); Li7Si3/Li13Si4 (158 мВ); Li13Si4/Li21Si5 (44 мВ). Теоретическая удельная емкость для максимального количества лития, интеркалированного в кремний, составляет 4212 мАч/г [26]. В настоящее время это самая высокая известная возможная емкость сплава. Внедрение лития в олово (Sn) происходит в несколько этапов, подобно кремнию. При комнатной температуре они по большей части легко обнаруживаются в первом цикле, как показано на рис. 10 b. Теоретическая удельная емкость для Li4.4Sn составляет 993 мАч/г.
![]() Рисунок 10. (a) Внедрение лития в кремний и олово (Sn), (b) Внедрение лития в Sn, измеренное при двух различных температурах [28].
Рисунок 10. (a) Внедрение лития в кремний и олово (Sn), (b) Внедрение лития в Sn, измеренное при двух различных температурах [28].
Большое количество лития образует сплавы с кремнием и оловом, что приводит к большому изменению объема во время интеркаляции/деинтеркаляции. Это, в свою очередь, вызывает потерю четко определенных этапаов внедрения во время циклирования и приводит к аморфизации материала [27]. Это разрушение кристаллической структуры похоже на внутреннее «шлифование», что значительно снижает стабильность циклирования. Для уменьшения этого эффекта используются чрезвычайно мелкие частицы (вплоть до нанодиапазона) (рис. 11 а). Дальнейшее улучшение стабильности циклирования достигается за счет использования в основном углеродных композитов; например, наночастицы встраиваются в углеродные или графитовые матрицы. Однако это снижает удельную емкость.
![]() Рисунок 11. (а) Влияние размера частиц кремния на циклирование по сравнению с теоретической емкостью для графита [29], (b) Влияние связующего агента на циклическую стабильность анодов на основе C/Si [30].
Рисунок 11. (а) Влияние размера частиц кремния на циклирование по сравнению с теоретической емкостью для графита [29], (b) Влияние связующего агента на циклическую стабильность анодов на основе C/Si [30].
В другом подходе для повышения стабильности циклирования используются химически активные связующие вещества. Они обеспечивают дополнительную стабилизацию композитного анода (рис. 11 b).
Титанат лития как анодный материал
Титанат лития (LTO), который кристаллизуется в виде шпинели (Li4Ti5O12), обратимо интеркалирует литий при 1.55 В (рис. 12 a) и достигает обратимой емкости около 160 мАч/г (Li7Ti5O12). Интеркаляция/деинтеркаляция лития практически не приводит к изменению объема частиц в этом процессе. Весь процесс состоит из двух фаз с отчетливым плоским плато в пределах окна стабильности электролита. SEI не образуется, а импеданс акуумулятора очень низкий. Все эти параметры являются причиной очень хорошей циклической стабильности аккумулятора (рис. 12 b) и высоких характеристик безопасности.
Недостатком этого материала является его очень низкая электропроводность и, как следствие, относительно плохая производительность. Следовательно, частицы должны быть как можно меньше, предпочтительно в нанодиапазоне, и дополнительно покрыты проводящим углеродом. Эти меры повышают мощность и срок службы титаната лития. Тем не менее, его плотность энергии остается низкой из-за низкой удельной емкости и высокого уровня потенциала vs Li/Li+ (рис. 1). Поэтому титанат лития особенно подходит для больших аккумуляторных ячеек в стационарных приложениях или для аккумуляторов в областях с очень высокими требованиями к мощности (например, гибридные автомобили).
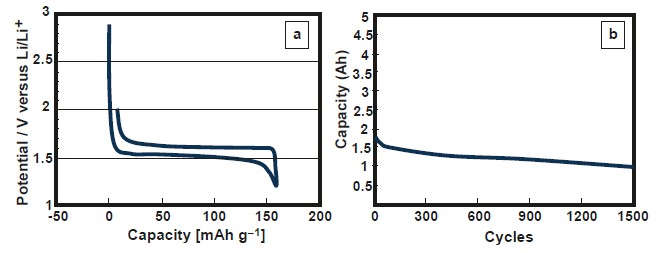 Рисунок 12. (a) Гальваностатическая кривая титаната лития (LTO) с металлическим литием в качестве противоэлектрода и (b) циклирование титаната лития при 60 °C [31]
Рисунок 12. (a) Гальваностатическая кривая титаната лития (LTO) с металлическим литием в качестве противоэлектрода и (b) циклирование титаната лития при 60 °C [31]
Анодные активные материалы – перспективы
Таблица 1: Качественная оценка характеристик наиболее важных анодных активных материалов. Данная оценка представляет собой лишь краткий обзор, который необходимо обновлять по мере развития активных материалов и системы литий-ионных аккумуляторов, поскольку в настоящее время во всем мире проводятся интенсивные исследования.
| Параметр | Энергия | Можность | Срок службы | Безопасность |
| Анодный материал | ||||
| Синтетический графит | ++ | + | + | + |
| Природный графит | ++ | + | 0 | 0 |
| Аморфный углерод | 0 | ++ | ++ | ++ |
| Титанат лития | -- | +++ | +++ | +++ |
| Композит C/Si или C/Sn | +++ | + | - | 0 |
| Сплавы кремния | ++++ | + | -- | - |
| Литий | ++++ | - | - | -- |
В таблица 5.1 представлено качественное сравнение основных характеристик наиболее важных анодных активных материалов, таких как энергия, мощность, срок службы и безопасность. Эта оценка отражает уровень знаний авторов на момент написания работ и просто дает основу для приблизительной ориентации и классификации рассматриваемых материалов. Принимая во внимание вышеупомянутые характеристики, в настоящее время наиболее важными анодно-активными материалами (в зависимости от области применения) являются следующие материалы: синтетический графит, природный графит (natural graphite), аморфный углерод (твердый и мягкий углерод/hard и soft carbpn) и титанат лития. Графит обладает наиболее сбалансированным профилем свойств и, как следствие, на сегодняшний день занимает наибольшую долю рынка. Однако композиты (в этом контексте в основном C/Si), скорее всего, приобретут большее значение в долгосрочной перспективе в зависимости от развития отрасли. Примерами таких материалов являются кремниевые сплавы, некремниевые сплавы, такие как сплавы на основе олова, и металлический литий. На рис. 13 представлена общая информация о текущем состоянии сырья для литий-ионных аккумуляторов [32].
 Рисунок 13. Карта поставок сырья для литий-ионных аккумуляторов [32].
Рисунок 13. Карта поставок сырья для литий-ионных аккумуляторов [32].
Ссылки:
- K.M. Abraham, Directions in secondary lithium battery research and development, Electrochimica Acta, Volume 38, Issue 9 , June 1993, Pages 1233-1248
- Matsuda Y (1989) Nihon Kagaku Kaishi 110:1
- E. Peled, The Electrochemical Behavior of Alkali and Alkaline Earth Metals in Nonaqueous Battery Systems—The Solid Electrolyte Interphase Model, J. Electrochem. Soc, 1979, 126, 2047
- Bolloré
- Armand M (1980) In: Broadhead J, Steele BCH (ed.) Materials for advanced batteries. Plenum Press, New York, pp. 145 – 150
- Nishi Y (1998) In: Wakihara M, Yamamoto O (eds.) Lithium ion batteries. Wiley-VCH, New York, p. 181
- Sid Megahed, Bruno Scrosati, Lithium-ion rechargeable batteries, Journal of Power Sources, 1994, Volume 51, Issues 1–2, August–September, Pages 79-104
- Dahn JR et al. (1994) In: Pistoia G (ed.) Lithium batteries–new materials, developments, and perspectives, industrial chemistry library. Elsevier, Amsterdam, pp. 1 – 47
- M Broussely, P Biensan, B Simon, Lithium insertion into host materials: the key to success for Li ion batteries, Electrochimica Acta, 1999, Volume 45, Issues 1–2, 30 September, Pages 3-22
- Ulrich von Sacken, Eric Nodwell, Avtar Sundler, J.R. Dahn, Comparative thermal stability of carbon intercalation anodes and lithium metal anodes for rechargeable lithium batteries, Solid State Ionics, 1994, Volume 69, Issues 3–4, August, Pages 284-290
- Jossen A, Wohlfahrt-Mehrens M (2007) Overview on current status of lithium-ion batteries. In: 2nd International renewable energy storage conference, Bonn, 19 – 21 Nov 2007
- Castner JH (1893) GB 19089
- Acheson EG (1895) US 568 323, 1895
- Marsh H, Griffiths JA (1982) A high, resolution electron microscopy study of graphitization of graphitizable carbon. International Symposium on Carbon, Toyohashi, p. 81
- Omaru A, Azuma H, Nishi Y (1992) Sony Corp., Japan Patent Application: WO 92-JP238 9216026
- Sekai K, Azuma H, Omaru A, Fujita S, Imoto H, Endo T, Yamaura K, Nishi Y, Mashiko S, Yokogawa M, Lithium-ion rechargeable cells with LiCoO2 and carbon electrodes, Journal of Power Sources, 1993, Volume 43, Issues 1–3, 15 March , Pages 241-244
- Martin Winter, Jürgen O. Besenhard, Michael E. Spahr, Petr Novák, Insertion Electrode Materials for Rechargeable Lithium Batteries, Adv Mater, 1998, 10 (10), 725-763
- Stephen J. Harris, Adam Timmons, Daniel R. Baker, Charles Monroe, Direct in situ measurements of Li transport in Li-ion battery negative electrodes, Chemical Physics Letters, Volume 485, Issues 4–6, 26 January 2010, Pages 265-274
- E. Peled, The Electrochemical Behavior of Alkali and Alkaline Earth Metals in Nonaqueous Battery Systems—The Solid Electrolyte Interphase Model, J. Electrochem. Soc, 1979, 126, 2047
- F Orsini, L Dupont, B Beaudoin, S Grugeon, J.-M Tarascon, Scanning and transmission electron microscopy contributions to the improvement of electrode materials and interfaces in the design of better batteries, International Journal of Inorganic Materials, Volume 2, Issue 6, December 2000, Pages 701-715
- E. Peled, D. Golodnitsky and G. Ardel, Advanced Model for Solid Electrolyte Interphase Electrodes in Liquid and Polymer Electrolytes, J. Electrochem, Soc. 1997, 144. L208
- J. R. Dahn, Tao Zheng, Yinghu Liu, and J. S. Xue, Mechanisms for Lithium Insertion in Carbonaceous Materials, Science, 1995, Vol 270, Issue 5236pp. 590-593
- Yinghu Liu, J.S. Xue, Tao Zheng, J.R. Dahn, Mechanism of lithium insertion in hard carbons prepared by pyrolysis of epoxy resins, Carbon, Volume 34, Issue 2, 1996, Pages 193-200
- J.R. Dahn, W. Xing, Y. Gao, The “falling cards model” for the structure of microporous carbons, Carbon, Volume 35, Issue 6, 1997, Pages 825-830
- C. John Wen, Robert A. Huggins, Chemical diffusion in intermediate phases in the lithium-silicon system, Journal of Solid State Chemistry, Volume 37, Issue , May 1981, Pages 271-278
- W.J Weydanz, M Wohlfahrt-Mehrens, R.A Huggins, A room temperature study of the binary lithium–silicon and the ternary lithium–chromium–silicon system for use in rechargeable lithium batteries, Journal of Power Sources, Volumes 81–82, September 1999, Pages 237-242
- Pimpa Limthongkul, Young-Il Jang, Nancy J. Dudney, Yet-Ming Chiang, Electrochemically-driven solid-state amorphization in lithium–metal anodes, Journal of Power Sources, Volumes 119–121, 1 June 2003, Pages 604-609
- Robert A. Huggins, Lithium alloy negative electrodes, Journal of Power Sources, Volumes 81–82, September 1999, Pages 13-19
- Graetz J, Ahn CC, Yazami R, Fultz B, Highly Reversible Lithium Storage in Nanostructured Silicon, Electrochemical and Solid-State Letters, 6 (9): A194–97
- N. S. Hochgatterer, M. R. Schweiger, S. Koller, P. R. Raimann, T. Wöhrle, C. Wurm and M. Winter, Silicon/Graphite Composite Electrodes for High-Capacity Anodes: Influence of Binder Chemistry on Cycling Stability, Electrochem. Solid-State Lett., 2008, 11, A76
- K. Zaghib, M. Simoneau, M. Armand, M. Gauthier, Electrochemical study of Li4Ti5O12 as negative electrode for Li-ion polymer rechargeable batteries, Journal of Power Sources, Volumes 81–82, September 1999, Pages 300-305
- Pillot C (2011) The rechargeable battery market past and future. Batteries 2011, 28 – 30 Sept, 2011. Cannes
Связанные публикации в Базе знаний:
- Катодные материалы для литий-ионных аккумуляторов
- Электролиты для литий-ионных аккумуляторов
- Сепаратор для литий-ионного аккумулятора
- Функции связующих материалов для электродов аккумуляторов, анализ, классификация.
- Политетрафторэтилен как связующее для литий-ионного аккумулятора
- Медная фольга как токосъемник для отрицательного электрода литий-ионного аккумулятора




