Разработка перспективных литий-ионных аккумуляторов (далее ЛИА) напрямую зависит от правильного выбора электролитных систем, природа которых может значительно варьироваться. Электролит литий-ионного аккумулятора — это проводящая среда внутри литий-ионной батареи, которая обеспечивает перемещение ионов лития между положительными и отрицательными электродами во время циклов заряда и разряда. Наиболее перспективными являются именно жидкие электролиты (наряду с гелевыми), которые в настоящее время используются в массовом производстве литий-ионных аккумуляторов.
Состав каждого электролита для литий-ионных аккумуляторов включает три класса материалов: проводящие соли, органический апротонный растворитель (или частично полимеры) и дополнительные компоненты (или добавки), которые могут как улучшить физико-химические свойства электролитного раствора, так и повысить эффективность работы электродов.
Список требований к идеальному электролиту разнообразен и включает в себя следующие пункты:
- высокая проводимость в широком диапазоне температур (от − 40 °C до + 80 °C);
- стабильность в течение нескольких тысяч циклов;
- химическая и электрохимическая совместимость с электродом;
- безопасность;
- экологичность;
- экономичность.
Выполнение всех этих требований создает ряд проблем, которые могут быть преодолены только с помощью инноваций. Здесь стоит отметить, что “идеального” электролита пока не существует.
Компоненты электролита
Набор инструментов для каждого электролита для литий-ионных аккумуляторов состоит из трех классов материалов: электропроводящих солей, органических апротонных растворителей (или, частично, полимеров) и добавок. Именно сочетание этих компонентов во многом определяет физико-химические и электрохимические характеристики электролита и способствует достижению вышеуказанных целей.
Выбор растворителей
В соответствии с основными требованиями к электролиту можно установить минимальные критерии подходящего растворителя:
- растворитель должен растворять соли лития в достаточно высокой концентрации. Это означает, что он должен иметь высокую диэлектрическую проницаемость (ε), чтобы обеспечить соответствующую сольватация ионов;
- должен иметь низкую вязкость (η), чтобы обеспечить беспрепятственный транспорт ионов. Этот параметр играет важную роль при низких температурах и для приложений требующих высокого напряжения, где (говоря с микроскопической точки зрения) требуется достаточная скорость миграции ионов лития;
- растворитель должен быть инертен по отношению ко всем другим компонентам ячейки при всех условиях эксплуатации особенно в отношении материалов заряженных электродов и токосъемника;
- стабильность растворителя играет решающую роль. Подходящий растворитель должен обладать низкой температурой плавления и максимально высокой температурой кипения;
- кроме того, сохраняются требования, касающиеся безопасности (нетоксичность) и необходимо учитывать экономическую составляющую.
В литий-ионных аккумуляторах для отрицательного электрода используются материалы с высокой восстановительной способностью (в основном литированный углерод или графит) и высокоокисляемые компоненты для положительного электрода (в основном оксиды лития или фосфаты металлов). Это причина того, почему растворители с активным кислотным протоном непригодны. Это сразу же приводит к выделению водорода. По этой же причине исключается вода как растворитель.
В связи с этим два класса органических растворителей, одновременно апротонных и высокополярных, получили признание как подходящие материалы для литий-ионных аккумуляторов: эфиры и сложные эфиры, включая органические карбонаты. Хотя в технической литературе обсуждаются альтернативы такие как нитрил, функционализированные силаны, сульфоны и сульфиты. В настоящее время эти классы веществ представляют собой только академический интерес.
В таблице ниже приведены характеристики органических растворителей, являющиеся в настоящее время основными компонентами электролитов для литий и литий-ионных источников тока.
Электролиты, содержащие эфиры, в большинстве своем обладают низкой вязкостью и, следовательно, очень высокой проводимостью. Но их электрохимическая стабильность ограничена, и они уже окисляются при потенциалах около 4 В vs Li/Li+. Таким образом, с появлением оксидов переходных металлов c напряжением 4 В в качестве материалов для положительных электродов простые эфиры перестали использоваться в качестве растворителей для литий-ионных аккумуляторов с высокой энергией.
| Растворитель | Температура плавления, ºС | Температура кипения, ºС | Диэлектрическая константа, (25 ºС) | Вязкость, 10-3 Па·с |
| Этиленкарбонат, EC | 39 | 248 | 95.3 | 1.9 |
| Пропиленкарбонат, PC | -70 | 240 | 65.1 | 2.53 |
| Диметилкарбонат, DMC | 4 | 90 | 3.1 | 0.59 |
| Метилэтилкарбонат, MEC | -55 | 109 | 2.9 | 0.65 |
| Диэтилкарбонат, DEC | -43 | 126 | 2.8 | 0.75 |
| 1,3-Диоксалан, DOL | -95 | 75 | 7.1 | 0.59 |
| 1,2-Диметокстиэтан, DME | -58 | 84 | 7.2 | 0.45 |
| γ-Бутиролактон, GBL | -43.5 | 204 | 39.0 | 1.75 |
Сложные эфиры, особенно органические диэфиры карбоновой кислоты (так называемые карбонаты), находят широкое применение на современном уровне техники. Как правило, используются смеси циклических карбонатов (например, этиленкарбонат [EC] и, в некоторой степени, пропиленкарбонат [PC]), которые обладают высоким дипольным моментом при умеренной вязкости. Также используются карбонаты с открытой цепью (диметилкарбонат [DMC], диэтилкарбонат [DEC] и этилметилкарбонат [EMC]), которые обладают умеренным дипольным моментом при низкой вязкости.
Иногда в качестве сорастворителей добавляют сложные эфиры с открытой цепью, такие как этилацетат (EA) или метилбутират (MB), для дальнейшего улучшения низкотемпературных характеристик электролита.
Выбор проводящей соли
Хотя выбор растворителя остается актуальной задачей, существует также необходимость обратить внимание на выбор соли электролита. Подходящая литиевая соль должна отвечать основным требованиям:
- максимально растворяться и полностью диссоциировать в апротонных растворителях для обеспечения высокой подвижности литий-ионов;
- обладать высокой электрохимической стабильностью анионов, особенно в отношении окисления, плюс — высокой химической стабильностьюю по отношению к растворителю;
- обладать хорошей совместимостью со всеми компонентами элементов, особенно токосъемниками;
Этим требованиям соответствуют в основном сложные анионы, в которых отрицательный заряд в значительной степени делокализован. Эта пониженная плотность заряда, в свою очередь, приводит к низкому притяжению между анионом и катион лития, которое определяет свободное движение катиона.
Электроноакцепторные группы (простейшие: фтор, сложные: высокофторированные органические остатки, карбоксильные или сульфонильные группы) приводят к минимуму взаимодействия между анионом и катионом лития. Хотя химия в принципе допускает большое количество различных слабокоординирующих анионов, на практике их число намного меньше из-за причин стабильности, стоимости и обработки.
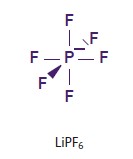
Гексафторфосфат лития. Что касается соединений, которые в принципе возможны, то гексафторфосфат лития (LiPF6) играет особую роль. В настоящее время коммерческие литий-ионные аккумуляторы изготавливаются почти исключительно с использовнием LiPF6. С одной стороны, это объясняется не какой-то одной выдающейся характеристикой, а уникальным сочетанием характеристик, не имеющим аналогов. А с другой стороны, это основано на готовности принять отдельные недостатки (таблица. 1).
Таблица 1. Профиль свойств LiPF6.
 |
Преимущества
|
|
Недостатки
|
С конца шестидесятых годов эта добавка уже используется в литиевых аккумуляторах в качестве проводящей соли. С годами процесс производства, качество и чистота, которые имеют решающее значение для работы батареи, совершенствовались. Например, высокочистый LiPF6 стал доступен в промышленных масштабах только с конца восьмидесятых годов. Современная технология по производству литий-ионных аккумуляторов была разработана на основе этой электропроводящей соли.
С самого начала его использования было хорошо известно, что LiPF6 обладает лишь ограниченной химической и термической стабильностью: в чистом виде она очень медленно распадается на следовое количесво фторида лития (LiF) и пентафторида фосфора (PF5), находящихся в равновесие. Это реаакция уже имеет место при комнатной температуре.
LiPF6 (газ, твердый) ⇔ LiF (твердый) + PF5 (газ)
Высокие температуры только способствуют этому процессу.
LiPF6 несколько более стабильна в органических растворах, например, в стандартных электролитах на основе органических карбонатов, но все равно распадается выше 70 °C. Сильная кислота Льюиса (PF5) инициирует несколько других реакций. Происходит медленная полимеризация, особенно в сочетании с циклическими органическими растворителями, что заметно по слегка желтому цвету электролита (Hazen > 50 APHA). Кроме того, LiPF6 чувствительна к гидролизу и вступает в реакцию с незначительными количествами воды, образуя плавиковую кислоту (HF).
LiPF6 + H2O ⇒ LiF + 2HF + POF3
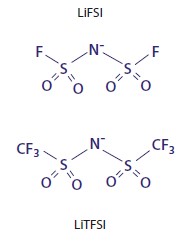
Бис(трифторметансульфонил)имид лития и Бис(фторсульфонил)имид лития и их производные. В последние годы на рынок все чаще стали выводится новые формулы. Это попытки заменить гексафторфосфат лития, поскольку он очень восприимчив к гидролизу. Наиболее перспективными подходами являются соединения на основе сульфонилимидов, например, литий-бис(трифторметилсульфонил)имид (LiTFSI) и бис(фторсульфонил)имид лития (LiFSI). Преимуществом этих новых электропроводящих солей является их проводимость, аналогичная проводимости LiPF6, и, следовательно, они удовлетворяют требованиям к высокому току нагрузки. LiFSI демонстрирует проводимость 12 мСм/см (0.85 М, 25 °C, EC/DMC). Это выше, чем у LiPF6, что делает ее особенно подходящей для высокотоковых применений. Проводимость LiTFSI немного ниже, чем у LiPF6 (таблица 2). Важную роль также играет диссоциация этих солей в широко используемых карбонатах.. Высокая степень диссоциации обеспечивает достаточно высокую проводимость и работоспособность аккумулятора даже при низких температурах.
Таблица 2. Профиль свойств бис(трифторметансульфонил)имид лития и Бис(фторсульфонил)имид лития.
 |
Преимущества
|
|
Недостатки
|
Как LiFSI, так и LiTFSI демонстрируют высокую термическую стабильность. Соль LiFSI гораздо более стабильна с температурой разложения более 200 °C, чем часто упоминаемый гексафторфосфат. Поэтому ее использование обеспечивает значительное улучшение безопасности эксплуатации. В начале 2013 года японская компания Nippon Shokubai ввела в эксплуатацию первую крупномасштабную установку для получения LiFSI с годовой производительностью от 200 до 300 т.
Однако с этими двумя соединениями существуют значительные проблемы. Так на катоде наблюдается повышенная коррозия алюминиевых токосъемников. Это локальное повреждение подложки вызвано недостаточным и нестабильным по потенциалу образованием пассивирующего слоя. Для LiTFSI оно начинается уже при напряжении около 3.7 В. В литературе упоминаются различные потенциалы начала окисления материала-носителя для LiFSI: токи деградации измеряются уже при 3.3 В, если материал загрязнен хлорид-ионами. Если материал имеет более высокую чистоту (меньшее загрязнение хлоридами), то это значение может быть выше 3.8 В.
Новые подходы для поиска проводящих солей
Фторалкилфосфат лития LIFAP. В конце девяностых годов был представлен новый класс проводящих солей для электролитов литий-ионных аккумуляторов - фторалкилфосфаты лития. Структура выдает его связь с LiPF6. С точки зрения структуры Li[PF3(C2F5)], LiFAP, происходит от LiPF6 путем замены трех перфторэтильных групп на соответствующие фторидные группы (в общем случае: перфторалкильные группы) (талица 3).
Таблица 3. Профиль свойств фторалкилфосфат лития.
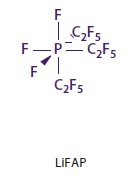 |
Преимущества
|
|
Недостатки
|
Значительная делокализация отрицательного заряда тремя перфторалкильными группами позволяет получать высокопроводящие электролиты, что, несмотря на размер групп, дополнительно приводит к небольшому повышению электрохимической стабильности. В настоящее время ведутся исследования, направленные на определение того, является ли LiFAP выгодным при использовании с современными электродными материалами c напряжением 5 В.
LiFAP не вступает в реакцию в присутствии воды с образованием плавиковой кислоты. Этот класс электропроводящих солей еще не освоен в промышленном производстве. Одной из причин является высокая молекулярная масса (для производства 1 литра электролита требуется в три раза больше LiFAP, чем LiPF6). Другая причина - это сложный и дорогостоящий производственный процесс. В настоящее время исследователи изучают альтернативные LIFAP соли с меньшим количеством перфторалкильных групп и меньшей молекулярной массой.
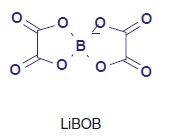
Биоксалатборат лития, LiBOB. Хелатобораты были разработаны для поиска экологически чистых альтернатив существующим проводящим солям. Они имеют бор в качестве центрального атома, и наиболее удачным вариантом является литий-бис(оксалато)борат (LiBOB). Его можно использовать в качестве функциональной добавки с исключительными характеристиками пленкообразования и в качестве нетоксичной, не вызывающей коррозии соли для специальных применений. Его оптимизированные характеристики пленкообразования могут быть использованы, например, для снижения доли этиленкарбоната (EC) в электролитах на основе карбонатов. EC используется специально с анодами на основе графита для формирования стабильной граничной поверхности SEI, которая, в свою очередь, предотвращает разрушение графитовых слоев из-за интеркалированных молекул растворителя (таблица 4).
Тавлица 4. Профиль свойств биоксалатборат лития.
 |
Преимущества
|
|
Недостатки
|
Характеристики пленкообразования не ограничиваются активными материалами анода. Они также наблюдаются на фольге катодного токосъемника. При разложении LiBOB, его типичные продукты распада вызывают пассивацию поверхности с помощью AlBO3. Этот слой достаточно стабилен, чтобы выдерживать потенциалы до 5 В. Проводящие соли, такие как LiFSI и LiTFSI, склонны к локальной коррозии поверхности алюминия, как описано выше. Добавки, такие как LiBOB, играют важную роль в достижении пассивации и, следовательно, значительном увеличении срока службы аккумулятора.
Есть еще одно преимущество использования LiBOB в качестве добавки в электролиты на основе LiPF6 для электродных материалов на основе марганца: он притягивает следы воды в готовом электролите. Это означает, что ингибируются диссоциация LiPF6 и последующее образование фтороводорода (HF).
Рис. 1 наглядно демонстрирует влияние LiBOB как добавки в электролиты на основе LiPF6: Добавление 2 % LiBOB уже приводит к снижению вымывания марганца примерно на одну единицу при хранении литий-марганцевой шпинели в следующих электролитах: чистый электролит с LiPF6, электролит с добавкой LiBOB и чистый электролит LiBOB. Скорость деградации чрезвычайно снижена в чистом электролите LiBOB.
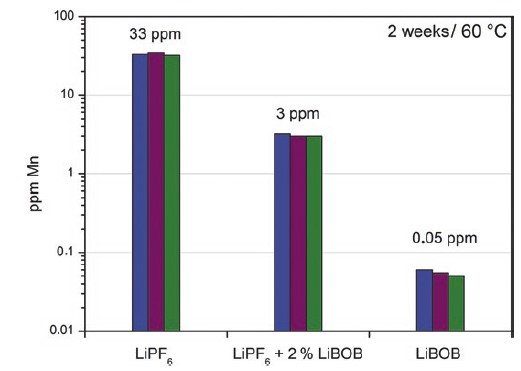 Рисунок 1. Скорость выделения марганца из литий-марганцевых шпинелей после хранения в соответствующих электролитах при повышенной температуре (EC/DEC 7:8).
Рисунок 1. Скорость выделения марганца из литий-марганцевых шпинелей после хранения в соответствующих электролитах при повышенной температуре (EC/DEC 7:8).
Функциональные электролиты
Помимо транспортировки ионов лития, электролиты должны выполнять дополнительные задачи для повышения безопасности и производительности.
Новые области применения литий-ионных аккумуляторов, такие как электромобили и стационарное хранение, предъявляют повышенные требования. Добавки здесь играют решающую роль в выполнении этих требований.
Срок службы аккумулятора и стабильность при циклировании
Образование пленки SEI на отрицательном электроде. Добавки в основном используются для оптимизации так называемого поверхностного пассивирующего слояа (SEI), граничной поверхности между отрицательным электродом и электролитом. SEI существенно влияет на срок службы и производительность литий-ионного элемента.
Ионы лития существуют в органических полярных растворителях не в виде “голых” катионов, а в виде сложных аддуктов растворения катионов. Этот так называемый сольватный комплекс, который во много раз больше, чем "голый" ион лития.
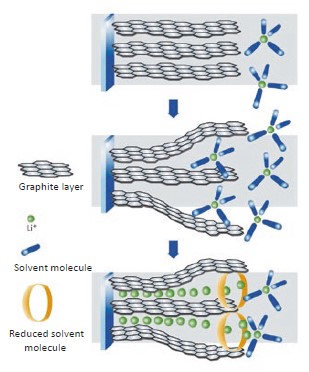
Сольватированные ионы лития проникают во внешние структуры графитового анода во время заряда литий-ионного аккумулятора (таблица 5). Растворители (и частично также анион литиевой соли) разрушаются из-за чрезвычайно восстановительных условий и образуют труднорастворимые осадки. Как правило, в органических карбонатах труднорастворимые образуются алкилкарбонаты лития Li[OC(O)OR] и Li2 [OC(O)O-(CHR)n-O(O)CO]. Они накапливаются на электроде и во внешних структурах графита и образуют слой, который называемый SEI.
Таблица 5. Механизм образования слоя SEI на отрицательном электроде.
 |
Формирование пленки SEI
|
Требования к SEI
|
Этот слой проницаем для ионов лития. В то же время он является электроизолирующим и предотвращает прямой контакт электрода и растворителя, что предотвращает дальнейшую деградацию растворителя. Кроме того, SEI десольватирует, т. е. от иона лития отрываются молекулы растворителя во время его прохождения и далее он диффундирует в электрод как "голый" катион.
Во время заряда графитовые слои значительно расширяются, а при разрядке элемента без SEI они сжимаются. Это так называемое “дыхание” может привести к “разрушению” электрода при увеличении числа циклов заряда и разряда и, следовательно, сократить срок службы аккумулятора.
Все карбонаты, используемые в настоящее время в литий-ионных аккумуляторах, образуют SEI. Однако качество и состав слоя сильно зависят от выбранной комбинации растворителей. Качество слоя SEI ухудшается в зависимости от восстановительного потенциала растворителя EC ≫ DMC > EMC > DEC ≫ PC.
Этиленкарбонат (EC) занимает особое положение в этом ряду: он образует высококачественный, т. е. электронно-пассивирующий слой SEI, который все еще проницаем для ионов Li+. Это связано с образующимися двухвалентными алкилкарбонатами лития Li2[OC(O)O – (CH2)n – O(O)CO]. Соответственно, почти во все используемые в настоящее время электролиты для аккумуляторов добавляется от 20 до 50 % EC.
Пропиленкарбонат (PC), с другой стороны, не образует подходящего SEI. PC менее подвержен восстановлению из-за индуктивного эффекта метильной группы. Вызванный этой стабильностью (потенциал восстановления вышепримерно на 200 мВ), PC, т. е. сольват Li+-PC, глубоко интеркалируется в графит и только затем распадается, образуя CO2. Это приводит к расширению и разрушению структуры графита.
Добавки могут оказывать существенное влияние на структуру и характеристики SEI. Основы подхода по поиску добавку для SEI просты. Добавки, способстьывующие образованию SEI, должны обладать более высокой электрохимической активностью, чем все остальные компоненты электролита. С другой стороны, SEI должен быть уменьшин во время первого цикла заряда литий-ионного элемента перед использованием растворителей. Таким образом, SEI образуется до того, как растворители вступят в реакцию.
Самым известным примером этого класса добавок является виниленкарбонат. Он используется почти в каждом коммерческом литий-ионном элементе и значительно повышает стабильность его работы. Он становится эффективным во время первых циклов заряда и разряда литий-ионного аккумулятора. Виниленкарбонат восстанавливается немного выше уровня интеркаляции Li+ в углерод при потенциалах около 1 ÷ 1.1 В
vs Li/Li+. На электроде образуется очень тонкая, полимероподобная (и, следовательно, гибкая) пленка.
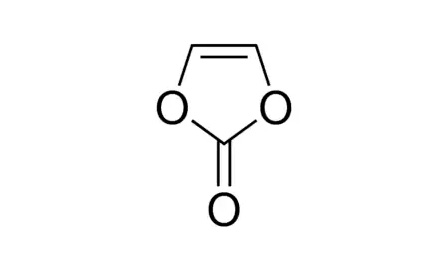
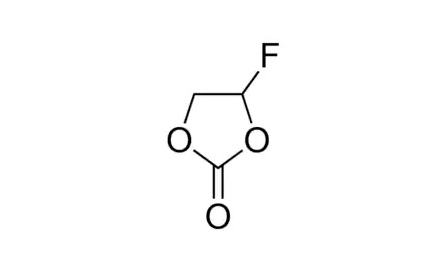
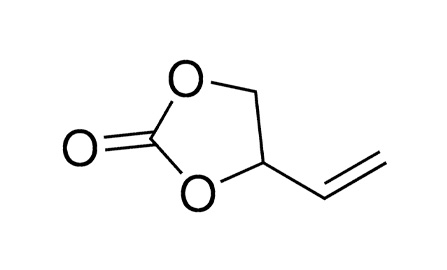
Существует множество альтернатив виниленкарбонату. Используются различные функционализированные органические карбонаты, например, фторэтиленкарбонат (FEC) и винилэтиленкарбонат (VEC). Но также используются SEI-образующие проводящие соли, такие как вышеупомянутый литий-бис(оксалато)борат (LiBOB). Все эти разработки все еще находятся в зачаточном состоянии (таблица 6).
Таблица 6. Добавки, образующие пленки SEI.
 |
 |
 |
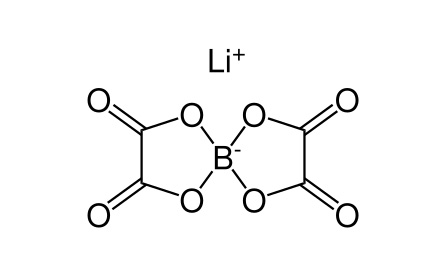 |
| Виниленкарбонат, VC | Фторэтилен карбонат, FEC | Винил-этилен карбонат, VEC | Биоксалатборат лития, LiBOB |
Использование LiBOB в качестве добавки является одним из примеров целенаправленного изменения структуры SEI: наблюдаются различные структуры в присутствии различных растворителей, которые проявляют различную реакционную способность на поверхности электрода. На граничной поверхности электролитов на основе EC преобладают продукты разложения EC. Причина в том, что эти электролиты имеют более высокую реакционную способность и, следовательно, более плотную структуру (рис. 2, слева). слой SEI в основном состоит из EC, даже когда используется LiBOB. Для растворов, не содержащих EC, ситуация иная (рис.2, справа): граничный поверхностный слой состоит из обоих компонентов. Образование пленки зависит от способа формования.
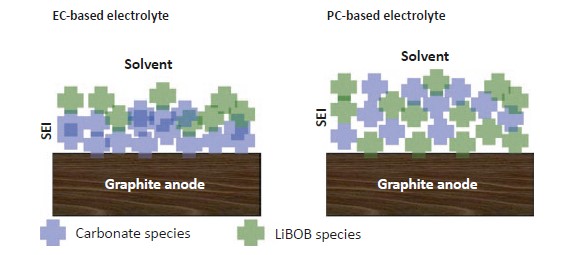 Рисунок 2. Влияние LiBOB на формирование пленки SEI.
Рисунок 2. Влияние LiBOB на формирование пленки SEI.
Образование пленки на положительном электроде. В течение последних 20 лет при разработке новых электролитов для литий-ионных аккумуляторов основное внимание уделялось химическим свойствам граничных поверхностей на отрицательном электроде, особенно на графитовом электроде.
Однако, теперь, пограничная поверхность между электролитом и положительным 5В электродом (например,высоковольтные шпинели или LiCoPO4) вышла на передний план. Целью данных исследованийя является разработка усовершенствованных литий-ионных аккумуляторов с еще более высокой плотностью энергии и электродных материалов для работы при 5 В. Можно предположить, что нет электролита, который был бы термодинамически стабилен при 5 В vs Li/Li+.Подходы, которые приводят к свойствам, сходными с образованиющими пленками SEI на отрицательном электроде, т.е. пассивация положительного электрода путем окислительного разложения специальных добавок, в настоящее время представляются наиболее перспективными.
Эти исследования, однако, все еще находится в зачаточном состоянии. В первых публикациях потенциальными пленкообразователями назывались специальные бораты и оксиды бора. Другие авторы уделяют особое внимание добавкам, которые добавляются в электролит в заметно низких концентрациях (< 0.1 %) и которые электрополимеризуются на электроде при напряжениях около 4.5 В vs Li/Li+. Примерами могут служить бифенил (BP) и его производные. В более высоких концентрациях (2 % и выше) эти добавки могут также использоваться для защиты от перезаряда.
Безопасность и защита от перезаряда
Не в последнюю очередь из-за аварий с электровелосипедами и возгорания ноутбуков вопросы о будущем литий-ионных аккумуляторов неразрывно связаны с вопросами безопасности. Существенной проблемой является поведение аккумулятора во время перезаряда. Чрезмерный заряд литий-ионного аккумулятора может привести к неконтролируемому нагреву элемента. Так называемый “тепловой разгон” в худшем случае может привести к разрыву элемента и его возгоранию.
Крайне важно предотвратить подобные события. Для достижения этой цели в электролитах используются такие добавки, как бифенил и циклогексилбензол, а также конструктивные решения, например, предохранительные клапаны и активное охлаждение. В обычных условиях эксплуатации литий-ионных элементов эти добавки инертны. Однако они активируются электрохимическим путем, когда напряжение в элементе достигает критического значения.
Например, бифенил электрополимеризуется при напряжении выше 4.5 В. В ходе этой полимеризации образуется изолирующий слой на положительном электроде. В то же время в контролируемом режиме происходит выброс большего количества газа, что приводит к открытию предохранительного клапана (рис. 3, слева). Это предотвращает дальнейшую неконтролируемую перезарядку элемента. Эти так называемые “отключающие” добавки имеют недостаток: после их использования аккумулятор становится непригодным для использования.
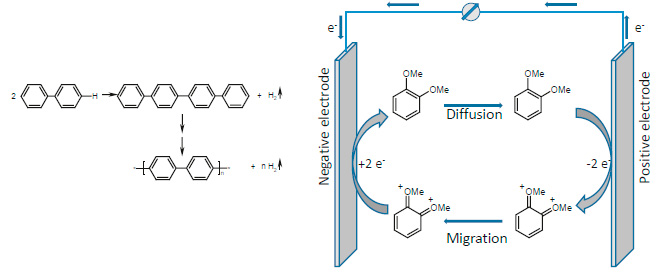 Рисунок 3. Механизм "Shut-down" (слева) и "redox shuttles" (справа).
Рисунок 3. Механизм "Shut-down" (слева) и "redox shuttles" (справа).
Сегодняшние исследования интенсивно направлены на поиск концепций, которые не проявляют этот недостаток «отключающих» добавок. Так называемые «redox shuttles» вызвали любопытство многих исследователей (рис. 3, справа). Как и “отключающие” добавки, этот класс добавок активируется при напряжении, превышающем напряжение заряда литий-ионного элемента.
Название «redox shuttles» говорит обо всем: добавка окисляется на положительном электроде и перемещается в электрическом поле к отрицательному электроду, где восстанавливается. Затем она диффундирует к положительному электроду, и процесс начинается сначала. Добавка “переносит” заряд через литий-ионный элемент посредством окислительно-восстановительной реакции. Функциональные возможности «redox shuttles», таких как галогенированные диметоксибензолы, уже задокументированы, но все еще нуждаются в большом объеме исследований. Современные окислительно-восстановительные системы еще недостаточно быстродействующие, чтобы надежно предотвратить тепловой разгон. В дополнение к этому, окислительно-восстановительные добавки могут использоваться только в системах с 3-вольтовыми аккумуляторами из-за их относительно низкого “напряжения активации”. Окислительно-восстановительные добавки для 4-вольтовых систем играют важную роль в текущих исследованиях.
Составы электролитов – индивидуальные и неповторимые
Как правило, не существует такого понятия, как “лучший электролит”. В большинстве случаев усовершенствования в одной области приводят к потерям в другой. Поэтому решения для электролитов всегда должны соответствовать требованиям заказчика и/или области применения. Например, требования к литий-ионному аккумулятору в мобильном телефоне отличаются в отношении срока службы от требований к тяговому аккумулятору в электромобиле.
Литий-ионный аккумулятор, как правило, выбирается с учетом требований к сроку службы, количеству циклов, старению, стабильности высокого тока, низкотемпературным и высокотемпературным характеристикам.
Электролиты для литий-ионных аккумуляторов в настоящее время состоят из двух-четырех различных растворителей. Такой подход к использованию “смешанных растворителей”, как правило, позволяет удовлетворить самые разные требования, например, низкую вязкость при одновременной высокой диэлектрической проницаемости, путем смешивания растворителей с различными физико-химическими характеристиками. Это отличается от использования проводящих солей, где смешивание производится крайне редко. С одной стороны, количество подходящих анионов ограничено. С другой стороны, преимущество соли еще предстоит доказать.
В настоящее время этиленкарбонат является компонентом растворителя практически для всех коммерческих электролитов для литий-ионных аккумуляторов с отрицательным электродом на основе углерода. Этот растворитель обладает очень хорошими характеристиками пленкообразования SEI и обеспечивает очень эффективную пассивацию графитового электрода. Кроме того, благодаря своей высокой диэлектрической проницаемости он позволяет получать электролиты с высокой проводимостью. EC имеет очень высокую температуру плавления 36 °C. Электролиты, основанные исключительно на 1 М LiPF6 и EC, остаются твердыми при комнатной температуре.
Как правило, стандартные смеси, используемые в настоящее время, состоят из 20 ÷ 50 % EC и карбонатов с открытой цепью (DMC, DEC или EMC) или эфиров (EA или MB). В зависимости от соотноешения при смешивания, эти смеси обладают интересными значениями проводимости, значениями электрохимической стабильности и характеристики образования пленки в интервале температур от - 30 и + 80 °C. Аналогичных рекомендаций по выбору и концентрации добавок не существует. Их выбор всегда осуществляется на заказ. Здесь производителям электролитов и элементов питания необходимо очень тесно сотрудничать
Часто выбор подходящих добавок определяется методом “проб и ошибок”, а также требованиями заказчика, которые особенно влияют на определение оптимальной концентрации добавки. Это связано с тем, что у производителей элементов разные требования. Но дело не только в этом, даже в том, что их элементы различаются (цилиндрические, призматические, паучи, в твердом корпусе) в зависимости от соотношения электролита и электродного слоя. Принцип “чем больше, тем лучше” здесь не подходит. Как раз наоборот: слишком большое количество добавки в большинстве случаев является недостатком.
Прогноз
Электролиты являются важным компонентом литий-ионного аккумулятора. Взаимодействие растворителя, электропроводящей соли и соответствующих добавок образует сложную систему. Выбор этой системы должен быть тщательным, а ее характеристики должны сочетаться наиболее эффективным образом. В то же время электролит не является самостоятельным компонентом аккумулятора. Его необходимо выбирать в зависимости от материалов для анода и катода. Это, в свою очередь, требует тесного сотрудничества между производителем электролита и разработчиками элементов и батарей.
Новые проблемы связаны с новыми материалами для аккумуляторов следующего поколения, например, высоковольтными катодами, для которых требуются достаточно стабильные электролиты, не проявляющие склонности к разрушению даже при таких величинах потенциала. В дополнение к этому, эти электролиты должны обеспечивать пассивацию токоприемников, что является сложной задачей на стороне катода при более высоких потенциалах.
Наряду со всеми этими технологическими требованиями, для реализации будущих применений в области электромобилей и стационарных накопителей энергии необходимо быть уверенным в том, что необходимое количество действительно может быть произведено.
Ссылки:
- Kang Xu, Nonaqueous liquid electrolytes for lithium-based rechargeable batteries. Chem Rev, 2004, 104:4303 − 4417
- M Schmidt, U Heider, A Kuehner, R Oesten, M Jungnitz, N Ignat’ev, P Sartori, Lithium fluoroalkylphosphates: a new class of conducting salts for electrolytes for high energy lithium-ion batteries, J Power Sources, 2001, 97-98, 557 - 560
- Doron Aurbach, Yair Ein‐Eli, Boris Markovsky, Arie Zaban, S. Luski, Y. Carmeli and H. Yamin, The Study of Electrolyte Solutions Based on Ethylene and Diethyl Carbonates for Rechargeable Li Batteries: II . Graphite Electrodes, J. Electrochem. Soc., 1995, 142, 2882
- Ue M (2009) Electrolytes: nonaqueous in encyclopedia of electrochemical power sources. In: J.Garche (ed.) Elsevier B.V 71 − 84
Связанные публикации в Базе знаний:
- Анодные материалы для литий-ионных аккумуляторов.
- Катодные материалы для литий-ионных аккумуляторов.
- Сепаратор для литий-ионного аккумулятора
- Гексафторфосфат лития, как материал для электролита литий-ионных аккумуляторов
- Функции связующих материалов для электродов аккумуляторов, анализ, классификация.
- Как изготавливаются литий-ионные аккумуляторы?




